Стратегия здоровья.
С точки зрения химии, человеческий организм представляет собой 30-процентный водный раствор, насыщенный различными простыми и сложными молекулами, и который находится в их определённом балансе. Неадекватное минеральное состояние водной среды организма может быть одной из основных причин наиболее распространённых заболеваний человека, а кроме того, способно усугублять их.
Кислотность и щёлочность организма. Химия биологических процессов отличается от химии неживой природы тем, что реакции в ней протекают управляемо, при помощи специфических белков – ферментов.
Присутствие ферментов позволяет многократно повышать скорость биохимических реакций, а иногда вообще делает их возможными. Кроме того, ферменты позволяют протекать определённым процессам только там, где они нужны в данный момент. Т.е. вместо хаоса они обеспечивают разумную управляемость этих реакций. Однако ферменты эффективно работают лишь в определённом диапазоне температуры и кислотности.
Для поддержания адекватной кислотности биологической среды необходим баланс между поступлением/производством отрицательно заряженых ионов и положительно заряженых (главным образом, протонов). Ключевую роль в поддержании здорового баланса между кислотностью и щёлочностью играют буферные системы, лёгкие и почки. Лёгкие через выдыхаемый воздух очень быстро удаляют из организма углекислый газ, который увеличивает кислотность крови. А почки регулируют кислотно-щелочной баланс более медленно, удаляя кислотные вещества через мочу.
В этой сложной системе соблюдения кислотно-щелочного баланса задействованы и некоторые другие механизмы. Например, белковые структуры организма, имеющие щелочные или кислотные группы, способны отдавать протоны или наоборот, временно принимать их на хранение. Кроме того, при увеличении концентрации в крови углекислоты, которая создаёт повышенную кислотность, увеличивается способность гемоглобина высвобождать кислород, который эту кислотность снижает. При этом также учащается дыхание, благодаря чему углекислый газ выводится за счёт усиления вентиляции лёгких. Увеличение или уменьшение производства органических кислот также способно в какой-то мере стабилизировать кислотность крови *.
То, в какую сторону будет склоняться кислотность тканей и органов организма, зависит не только от функции лёгких и почек, но также от поступления кислото- и щёлочеобразующих элементов с пищей и питьём * * * *. Щелочные пищевые источники в процессе метаболизма образуют катионы, т.е. положительно заряженные ионы натрия (Na+), калия (K+), кальция (Ca2+) и магния (Mg2+). А кислотные источники образуют анионы, т.е. отрицательно заряженные ионы, такие как фосфат (PO4–), сульфат (SO4–), хлорид (Cl–).
Продукты животного происхождения, такие как мясо, яйца и сыр, содержат много фосфора, серных аминокислот (цистеин, метионин и таурин) и катионных аминокислот (лизин и аргинин), что значительно увеличивает производство катионов. Кроме того, поваренная соль многократно усугубляет кислотную нагрузку, вызванную их потреблением *.
А продукты растительного происхождения, такие как зелень, овощи и, в меньшей степени, фрукты и орехи, содержат много калия, магния и кальция, что увеличивает производство анионов. Диета современного европейца создаёт ощутимый и стабильный дисбаланс в сторону кислот. По этой причине повышение кислотности организма (ацидоз) встречается в несколько раз чаще, чем повышение её щёлочности (алкалоз). Среди непищевых причин высокой кислотной нагрузки чаще всего называют психологический стресс.
Практически все дегенеративные состояния и заболевания, включая сердечно-сосудистые, диабет II типа * *, камни в жёлчном пузыре и почках * *, кариес, остеопороз *, артрит, жировая дистрофия печени *, хроническое заболевание почек * *, потеря мышечной массы * *, гипертония * и, наконец, общая смертность *, ассоциируются с повышенной кислотностью тканей организма *.
Повышенная кислотная нагрузка, вызванная закисляющими продуктами питания, является существенным фактором риска рака, в том числе рака груди. И наоборот, защелачивающая диета может оказывать защитное действие *. Сравнение нескольких групп женщин с различными моделями питания показывает, что в группе с наиболее кислотообразующей диетой, против группы с наиболее щёлочеобразующей диетой, риск ER– и TNBC подтипов рака выше, соответственно, в 1,7 и в 2,2 раза *.
Естественно, повышенная кислотная нагрузка увеличивает также уровень системного воспаления, что подтверждается значительным повышением уровня С-реактивного белка в плазме *. А воспаление, в свою очередь, стимулирует развитие рака. Т.о., кислотная нагрузка, вызванная пищей, может способствовать рецидиву заболеваний у женщин, которые успешно перенесли курс лечения *.
Кислотность крови, тканей и сред. Мера кислотности определяется показателем pH (potential hydrogen) *, который отражает количество протонов в растворе. Чем ниже показатель pH, тем кислотнее раствор, и наоборот. Шкала pH изменяется от 0 до 14, и является логарифмической, то есть, уменьшение значения pH на 1 единицу означает увеличение количества протонов (увеличение кислотности) в 10 раз. Нейтральным является значение pH, равное 7. Значения выше 7 являются щелочными, а ниже 7 – кислотными.

Различные участки в организме имеют значительные различия в показателях кислотности, и именно при тех, при которых ферменты, присутствующие в них, работают наиболее эффективно. Например, среда желудка, по сравнению с другими, очень кислая, чтобы можно было расщепить пищевой белок при помощи фермента под названием пепсин. А среда двенадцатиперстной кишки – наоборот, очень щелочная, для того, чтобы можно было расщепить жиры при помощи фермента под названием липаза.
Тем не менее, сами клетки обоих органов имеют нормальную внутриклеточную кислотность. Находясь в агрессивном окружении, они пытаются защищать себя, например, покрывая себя слизью, однако всё равно в массовом порядке гибнут, и вынуждены обновляться каждую неделю.
Как видим, кислотность клеток и кислотность окружающей их среды – это разные вещи. То же самое можно сказать про кислотность тканей и кислотность биологических жидкостей, про кислотность крови и кислотность тканей, про кислотность внутриклеточную и внеклеточную. Когда речь заходит о кислотности организма, имеется ввиду кислотность жидкости, окружающей клетки ткани. А не о кислотности крови, как это иногда пытаются представить.
Здоровый показатель кислотности артериальной крови человека составляет ~ 7,4±0,05 по шкале pH. Т.е. он несколько сдвинут в щелочную сторону относительно нейтрального показателя pH 7,0. Слегка щелочная среда крови обеспечивает достаточное снабжение клеток кислородом и их адекватный метаболизм. Показатель кислотности венозной крови – pH 7,36, такой же показатель кислотности во внеклеточной жидкости. Показатель нормальной кислотности внутри клеток ткани чуть ниже – pH 7,1-7,3, однако он всё равно остаётся в щелочной области, чтобы иметь возможность нести кислород.
В ходе жизненных процессов в кровь попадает большое количество щелочных и кислотных веществ. В процессе дыхания образуется большое количество молекул CO2, молочная кислота, глутаминовая кислота и янтарная кислота. Из пищеварительного тракта всасываются органические кислоты, продукты брожения углеводов. В результате множества метаболических процессов образуются молекулы фосфорной (H3PO4), серной (H2SO4) и других сильных кислот. Усиленное образование кислотных продуктов метаболизма происходит также при нарушении углеводного, липидного и белкового обмена, когда в крови в больших количествах появляются кетоновые тела (ацетоуксусная и β-оксимасляная кислоты, ацетон).
Поступление закисляющих или защелачивающих веществ может сдвигать показатель кислотности химической среды в ту или иную сторону. Даже незначительное изменение рН среды вызывает изменение активности ферментов и нарушение нормального течения биохимических процессов. Клетки млекопитающих жизнеспособны в довольно узком диапазоне кислотности крови (pH 6,8-7,8). Выход за пределы этих значений приводит к необратимым повреждениям и смерти клеток и всего организма. Допустимые физиологические колебания кислотности крови ещё уже – 0,05-0,07 единицы pH. Поскольку кислотность крови имеет жизненно важное значение, она является, наверное, наиболее строго поддерживаемым параметром. Чтобы держать кислотность крови в нужных пределах, организм использует некоторые механизмы стабилизации кислотности крови в организме.
Быстрое реагирование на возмущающий кислотный или щелочной фактор происходит за счёт присутствующих в крови химических веществ, которые называются буферы. Щелочные буферы моментально гасят внезапно возникшую избыточную кислотность, а кислотные буферы – избыточную щёлочность. Типичным примером минерального щелочного буфера является обычная пищевая сода, а органического щелочного буфера – гемоглобин, содержащиеся в крови в достаточном количестве. Они снижают кислотность быстро и непосредственно, путём прямой химической реакции. Тем временем почки, если они не перегружены и адекватно работают, понемногу удаляют кислотные продукты вместе с мочой. Когда же кислот производится больше, чем почки могут их вывести, наступает состояние, называемое метаболический ацидоз.
Буферные запасы в крови достаточно велики, чтобы справляться с обычными кислотно-щелочными возмущениями. У здоровых людей механизмы обеспечения гомеостаза способны поддерживать стабильный уровень ионов водорода или бикарбоната при кислотной нагрузке не выше ~ 1 ммоль/кг в сутки. Более высокие кислотные нагрузки, которые создаёт современная диета, приводят к некоторому повышению уровня кислот в крови, хотя и в пределах диапазона, считающегося нормальным * *. Это даёт основание для заявлений, что кислотная нагрузка, вызванная диетическим фактором, несущественна. Однако это не совсем верно.
Действительно, разовая кислотная нагрузка может быть вполне безопасной. Однако хроническое состояние повышенной кислотности крови, даже в пределах значений, считающихся «нормальными» (pH 7,35-7,4), будет действовать пагубно через ряд механизмов. Высокая кислотная нагрузка способствует повреждению, болезням и снижению функций почек *, что обычно проявляется и прогрессирует с возрастом *. По этой причине возможности почек удерживать адекватную стабильность кислотности крови падают. Таким образом, задача нейтрализации избыточной кислотности всё больше перекладывается на щелочные буферы.
Однако запасы буферов, растворённых в крови, не безграничны. Когда они начинают исчерпываться, нейтрализующие кислотность вещества заимствуются кровью из других источников, включая межклеточную жидкость и другие биологические жидкости, а также мягкие ткани и кости. Например, такие элементы, как кальций, извлекаются из костной ткани, а натрий – из печени и желудка. Подсчитано, что количество кальция, постепенно теряемого с мочой при современной «западной» диете, может составить 480 г за 20 лет, что соответствует почти половине всей скелетной массы кальция *.
Уменьшение запасов щелочных буферов (ацидоз) наблюдается при некоторых заболеваниях (сердечной недостаточности, рахите и т.д.), а также при кетозах, например при кетогенной диете. Если ацидоз не компенсируется, то рН крови будет смещаться в кислую сторону.
Истощение запасов щелочных буферов в тканях означает, что кислотные продукты метаболизма не будут нейтрализовываться, а будут присутствовать или накапливаться в межклеточном пространстве тканей, увеличивая их кислотность. С другой стороны, избыток кислотных метаболитов может сбрасываться в ткани, чтобы избежать их избытка в крови. Обе эти тенденции делают ткани организма более кислыми, вызывая симптомы хронической усталости, разбитости, слабой мышечной и суставной боли. Длительное закисление всего организма будет способствовать кариесу, остеопорозу, болезням суставов и низкоуровнему системному воспалению.
Кислотность ткани оказывает решающее влияние также на появление и развитие опухолевых процессов. Повышение кислотности межклеточного пространства приводит к ослаблению активности большинства ферментов, снижению насыщенности кислородом, усилению гликолизного производства энергии и падению иммунитета. Кислотность также влияет на способность организма усваивать минералы и питательные вещества, наиболее распространённым примером чего является дефицит йода.
Повышение внеклеточной кислотности, видимо, стимулирует клетки в качестве защитной меры увеличивать свою внутриклеточную щёлочность, что способствует процессам деления клеток и является первым шагом в цепи их злокачественных преобразований.
Изменение кислотности в эпителиальных тканях меняет также состав естественно присутствующей в них микрофлоры, потому что различные виды бактерий процветают при различной кислотности. Это, в свою очередь, нарушает здоровое сотрудничество хозяина и гостей, ухудшая состояние микросреды тканей. Кроме того, повышенная кислотность существенно ослабляет терапевтический эффект многих химиопрепаратов, например, доксорубицина, и наоборот *.
Чрезмерное защелачивание (алкалоз) тоже может наблюдаться у некоторых людей. Однако, как у пожилых людей, так и у больных раком чаще наблюдается ацидоз, чем алкалоз. Знание уровня кислотности организма имеет большую ценность для оценки общего здоровья. Как ни странно, уровень кислотности организма иногда определяют через кровь, хотя, как было обсуждено выше, такое измерение будет совершенно некорректным. Более правильным является измерение величины кислотности слюны, которая будет ближе к величине кислотности тканей организма, чем величина кислотности крови.
К сожалению, важность кислотно-щелочного равновесия тканей практически игнорируется современной медицинской наукой. Работ, посвящённых низкоуровневому хроническому ацидозу, опубликовано на удивление мало. В добавок к этому, многие популяризаторы науки подменяют понятие «кислотность ткани» понятием «кислотность крови», тем самым вводя своих слушателей в заблуждение и дискредитируя важность нормализации кислотности организма.
Кислотно-щелочной реверс
Средние показатели внутриклеточного pH (pHi) раковых клеток примерно на 0,1-0,2 единицы выше, чем показатели нормальных клеток, независимо от органа тела *. А средние показатели внеклеточного pH (pHe) в опухолях обычно на 0,3-0,7 единицы ниже, чем в нормальных тканях *. Т.е. суммарно, разница между pHe и pHi может измениться на целую единицу.

Даже незначительное изменение соотношения pHe/pHi может серьёзным образом повлиять на многие биологические и химические процессы в клетках * * и, в конечном счёте, привести к пролиферации, агрессивности и миграции раковых клеток *. Временное снижение внутриклеточной кислотности наблюдается во время митоза, благоприятствуя процессам деления клетки. Однако в случае злокачественной опухоли оно становится хроническим и, по-видимому, является самым ранним и решающим фактором злокачественных перерождений *.
В целом, сниженная внутриклеточная кислотность при повышенной кислотности опухолевой микросреды способствует переходу от предракового заболевания молочных протоков к инвазивному раку молочной железы *. А повышенная внеклеточная кислотность усиливает способность раковых клеток к вторжению, миграции и метастазированию.
Высокая внутриопухолевая кислотность придаёт раковым клеткам устойчивость к значительной части слабощелочных химиотерапевтических лекарств (таких, как доксорубицин и винбластин); снижает кислородонасыщение опухоли; вызывает повышенную активность насосов, удаляющих внутрь клеток лекарственные препараты; ослабляет действие большинства ферментов и препятствует иммунному поражению раковых клеток * *.
Рак не может существовать в щелочной, богатой кислородом среде, где осуществляется нормальная работа ферментов и иммунных клеток. Поэтому восстановление естественного кислотно-щелочного равновесия открывает новое перспективное направление профилактики и лечения рака – недорогое, целевое и совместимое практически со всеми используемыми в настоящее время химиотерапевтическими протоколами.
Кислотно-щелочная коррекция при раке может включать как внутриклеточное закисление раковых клеток, так и внеклеточное защелачивание опухолевой ткани. Она может осуществляться как косвенно – за счёт использования средств, подавляющих удаление из клеток положительных ионов, так и непосредственно – за счёт введения закисляющих или защелачивающих средств.
Внутриклеточное закисление раковых клеток и доведение внутриклеточной кислотности до нормального уровня приводит к замедлению их роста и значительной потере ними раковых характеристик.
Внутриклеточное закисление может достигаться блокировкой оттока из клетки положительных ионов (катионов), благодаря чему соотношение pHe/pHi может увеличиться, и выйти к норме. Дальнейшее (чрезмерное) внутриклеточное закисление способно привести клетки к кислотному стрессу, и даже к её гибели.
Эта задача, однако, затруднена тем, что клетки используют несколько альтернативных механизмов удаления кислотных метаболитов. Блокировка только одного из них может быть компенсирована усиленной работой остальных. Следовательно, для эффективного внутриклеточного закисления (снижения показателя pH) требуется комбинация веществ, ингибирующих наиболее активные экспортёры катионов.
Для кратковременного курса (1-3 месяца) – как в качестве самостоятельной, так и в качестве дополняющей терапии, может быть рассмотрена комбинация следующих испытанных практикой нетоксичных веществ:
• Целекоксиб (200 мг/сут) ацетазоламид, противовоспалительное средство – как ингибитор карбоангидразы (CAIX);
• Омепразол (10 мг/сут), противоязвенное средство – как ингибитор протонного насоса (H+/K+-АТФазы);
• Кверцетин (2 г/сут), пищевой компонент – как слабый ингибитор транспортёра молочной кислоты 1;
• Симвастатин (20 мг/сут), антихолестериновое средство – как слабый ингибитор транспортёра молочной кислоты 4;
• Амилорид (5 мг/сут), калийсберегающий диуретик – как ингибитор натрий-протонного обменника (NHE);
• Фенитоин (100 мг/сут), противосудорожное средство – как ингибитор потенциал-зависимого натриевого канала (VGSC).
Внеклеточное защелачивание опухолевой зоны может достигаться не только за счёт удержания катионов в клетках, но и их внеклеточной нейтрализацией, а также усилением кровоснабжения и, как следствие, улучшением доставки внутрь опухоли щелочных элементов. Увеличение потребления естественных физиологических щелочных буферов способно поднять уровень pH в опухоли без заметного влияния на pH нормальной ткани, а тем более – крови *.
• Бикарбонат натрия (до 35 г/сут *) - пищевая сода (NaHCO3), выглядит наилучшим натуральным щелочным источником, который можно вводить как через рот, так и через инъекции. Для приёма внутрь берут 1 чайную ложку соды на 0,5-1 стакан воды до 5 раз в день * * за 30 минут до еды или через 2 часа после неё. Дозировка бикарбоната не должна повышать показатель pH мочи более, чем 7,5-8.
Бикарбонат соединяется с протоном (ионом водорода), образуя воду и углекислый газ – нетоксичные эндогенные продукты, которые легко выводятся из организма. У мышей с привитой ER– метастатической опухолью молочной железы, потребление соды с питьевой водой (в человеческом эквиваленте 12,5 г бикарбоната в сутки) избирательно повышало pH внеклеточной жидкости в опухоли, а также уменьшало образование спонтанных метастазов * и увеличивало выживаемость животных *. Но несмотря на это, пероральное применение одного лишь бикарбоната в опытах на животных оказалось неспособным затормозить рост первичной опухоли.
Однако добавки бикарбоната в питьё у мышей вызывали внеклеточное защелачивание опухоли и приводили к значительному повышению терапевтической эффективности доксорубицина против привитой опухоли молочной железы (MCF-7) *. А внутрибрюшинные инъекции бикарбоната вызывали у мышей более чем 4,5-кратное увеличение гибели раковых клеток молочной железы при лечении их митоксантроном *.
• Цитрат натрия (до 35 г/сут *), бикарбонат калия, карбонат магния, карбонат кальция, аскорбат калия и их смеси оказывают аналогичное действие. Однако среди всех рассмотренных соединений только бикарбонат натрия является естественным щелочным буфером, не требующим дополнительного клинического изучения.
К сожалению, потребление внутрь такого большого количества пищевой соды не только вызывает отвращение, но также может привести к электролитному дисбалансу и негативным побочным эффектам из-за сильного избытка натрия. Избежать этого можно путём приёма сбалансированного комплекса внеклеточных (натрий, кальций, бикарбонат, хлорид) и внутриклеточных (калий, магний, фосфаты, сульфаты) электролитов.
Тем не менее, пероральное применение щелочных элементов выглядит сомнительным, ввиду большого количества кислотных буферов, присутствующих в крови, которое способно полностью погасить ощелачивающий эффект любых добавок. Более эффективным было бы доставлять щелочные средства местно, вместо того, чтобы перенасыщать ними весь организм. Скандально известный доктор Тулио Симончини (Tullio Simoncini) предлагал инъекционное введение бикарбоната натрия. Протокол его лечения был следующий
*:
- Представьте полукруг вокруг места опухоли, и отметьте точки, соответствующие 11:00 и 13:00 по циферблату.
- Ежедневно в течение 6 дней делайте в эти точки инъекцию 70-100 мл 5 %-ного бикарбоната натрия.
- После этого переходите к внутривенному введению 500 мл 5 %-ного бикарбоната натрия: 6 дней введения и 6 дней без него, всего 4 цикла.
- Через 1-2 месяца, если опухоль не исчезла полностью, повторите курс лечения.
- В случае усталости и жажды принимайте много минерализованой воды.
- Если появляется синяк или раздражение, сделайте перерыв в лечении в течение 1-2 дней.
- В случае упорства одного из них, делайте инъекцию вокруг него 5 %-ного бикарбоната натрия по 70-100 мл каждый день в течение шести дней.
Побочные эффекты: боль и отёк груди. Боль длится несколько минут, отёк – много дней или даже 1-2 месяца. Если в подмышечной впадине имеются ощутимые лимфатические узлы, они могут регрессировать после лечения.
Творческие инициативы Симончини не нашли широкой поддержки у медицинской общественности, а сам он был подвержен судебным преследованиям, которые были связаны со смертями пациентов, последовавших после применения его протокола лечения.
• Басенпулвер (Basenpulver®) – комплекс щелочных солей с широким диапазоном буферного действия. Содержит бикарбонат калия, ортофосфат кальция, ортофосфат магния, цитрат калия, цитрат кальция, цитрат магния, селенит натрия. Дозировка: 3-4 полных чайных ложки (25-30 г), растворённые в 2 стаканах воды, но не более. Раствор принимают не ранее, чем через 15 минут после приёма пищи, и запивают большим количеством воды. При появлении негативных побочных эффектов дозировка снижается. Меланомные мыши, получавшие водный раствор Basenpulver, снижали кислотность опухоли, и вдвое сокращали скорость роста объёма опухоли *.
• Мультифорс (Multiforce®) – мультиминеральный щелочной комплекс, который содержит бикарбонат калия, фосфат магния, цитрат калия, цитрат кальция, цитрат магния, дикальцийфосфат. Шесть чайных ложек комплекса обеспечивают полную суточную норму всех этих минералов независимо от того, сколько их принимается с пищей. Клиническое исследование показало, что ежедневный приём 2 чайных ложек (15 г) порошка Multiforce в течение месяца снижает у пациентов воспалительные явления остеоартрита, что может косвенно свидетельствовать о снижении кислотности тканей *.
• Католитная вода (т.н. «живая вода»). Электроактивированная щелочная вода снижает кислотность тканей и повышает активность метаболических процессов за счёт пониженной кислотности и повышенного отрицательного окислительно-восстановительного потенциала (ОВП) активированной воды. Величина ОВП характеризует способность вещества присоединять электроны; чем больше отрицательное значение ОВП воды, тем более богата она электронами и тем сильнее её антиоксидантная способность.
Электроактивированная щелочная вода вырабатывается на специальных установках из минерализированной воды и потребляется как дополнение, или взамен обычной питьевой воды, т.е. в объёмах 0,25-1 л/сут. ОВП электрически обработанной воды очень быстро падает, поэтому её принимают сразу же после приготовления.
Электрообработка воды при помощи электролизёра позволяет достигать показателя pH 9-10, что на порядок превышает показатель pH, достигаемый путём минеральных добавок; в частности, путём применения бикарбоната кальция (pH 8,5). Вода, собранная после электролиза у катода (отрицательного полюса), увеличивает концентрацию отрицательных ионов (анионов) в растворе. Мыши, потреблявшие электрически защелочённую воду с pH 10,5, показали торможение развития опухоли простаты, статистически сравнимое с мышами, потреблявшими бикарбонатную воду *.
Стоимость католитной воды в разы выше, чем бикарбонатной воды, а их терапевтический эффект примерно равнозначен *. Однако если католитная вода насыщает организм водородом, то бикарбонат натрия насыщает организм натрием, что будет негативно сказываться на балансе электролитов.
Точно так же, как и при использовании бикарбонатной воды *, терапевтический эффект электроактивированной воды оказался значительно слабее, чем её профилактический эффект. Для получения электроактивированной воды с показателем pH 10,5, в исходной воде растворяют NaCl и KOH в соотношении 1:300, однако использование вместо них мультиминеральных комплексов значительно обогатит электролитное разнообразие обработанной воды.
В отличие от минералонасыщенных смесей, рассмотренных выше, католитная вода обеспечивает щёлочность не за счёт щелочных минералов, а преимущественно за счёт насыщения воды щелочными ионами самой воды. Стоит предостеречь, что использование католитной воды с высоким показателем щёлочности может радикально снизить кислотность желудка, и тем самым серьёзно нарушить работу ЖКТ.
• Скорректированная диета с низким содержанием белка и с высоким содержанием калия и/или магния * может быть не менее успешна, чем ощелачивающие средства. Например, калий способен эффективно нейтрализовать избыточную кислотность за счёт образования KHCO3 или снижения содержания глютамина *. Анализ более 300'000 случаев заболеваний показывает, что риск заболеть раком поджелудочной железы снижается на 18 % с каждыми дополнительными 100 мг/сут магния *.
Несмотря на распространённый скептицизм, защелачивающая терапия демонстрирует положительный эффект в клинических исследованиях. Так, цитрат калия (40 mEq/сут) уменьшает потерю костной массы костной массы *, что косвенно может свидетельствовать о наполнении костной ткани щелочным буфером. Логично будет предположить, что остальные ткани организма, особенно пострадавшие от закисления, также улучшают свой кислотно-щелочной баланс.
Защелачивающая диета с дополнительным к химиотерапии пероральным приёмом бикарбоната натрия (3,0-5,0 г/сут) в 1,5-3 раза увеличивала среднюю общую выживаемость пациентов с запущенным раком поджелудочной железы, по сравнению с пациентами, получавших одну лишь химиотерапию * *. Здесь диета предполагала ежедневное потребление 400 г фруктов и овощей и отказ от мясных и молочных продуктов.
Наконец, ещё в 1984 году были проведены ограниченные неконтролируемые исследования на раковых пациентах, где в качестве защелачивающих средств использовались соли рубидия и цезия. Во всех случаях опухолевые массы исчезали *. К сожалению, за прошедшие с тех пор 37 лет эта дешёвая терапия так и не привлекла достойного внимания исследователей.
Комплексное управление кислотностью сочетает внутриклеточное закисление, внеклеточное защелачивание, а также митохондриальные и лизосомальные токсины, которые за счёт различных механизмов взаимно дополняют и усиливают действие друг друга. Поскольку мы видим двойное нарушение кислотных состояний (внеклеточное закисление и внутриклеточное защелачивание) , то и устранять их также следует одновременно.
Для усиления терапевтического действия к двум перечисленным выше спискам могут быть добавлены:
- митохондриальные токсины:• Доксициклин (100 мг/сут), антибиотик – как ингибитор производства митохондриального белка;
• Атоваквон (1'000 мг/сут)
*,
противо
• Метформин (500 мг/сут), сахароснижающее средство – как активатор производства молочной кислоты и ингибитор производства клеточной энергии;
- лизосомальные токсины:• Ципрофлоксацин (1'000 мг/сут), антибиотик – как ингибитор производства клеточной энергии и усилитель апоптоза.
Могут быть также использованы и другие лизосомальные ингибиторы, такие как хлорохин (chloroquine) или гидроксихлорохин (hydroxychloroquine) *.
Комплексное воздействие всех перечисленных элементов способно создать значительный кислотный стресс внутри опухолевых клеток, приводящий к подавлению их роста и апоптотической смерти. И одновременно с этим – к снижению внеклеточной кислотности, что может привести к уменьшению миграции, инвазии и метастазирования опухолевых клеток, а также к повышению кислородонасыщения и усилению действия химио- и иммунотерапии.
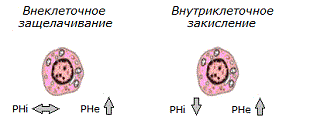
Остаётся, тем не менее, проблема доставки и насыщения опухоли действующими веществами, которая является следствием повышенного давления и плохого сосудистого потока жидкости внутри опухоли.
Электрофорез * может оказаться перспективным направлением снижения опухолевой кислотности. Отрицательные ионы, двигаясь под действием электрического поля, способны преодолевать механическое напряжение опухоли, и проникать внутрь неё, нейтрализуя кислотность ткани.
Для проведения процедуры электрофореза прокладку катода, смоченную раствором соды, размещают над опухолью, а прокладку анода, смоченную раствором минеральной воды – на противоположной стороне тела или, в случае неглубоко залегающей опухоли, на расстоянии до 10-15 см от катода. В результате прохождения постоянного электрического тока сквозь мягкие ткани, внутренние жидкости организма, которые на 70-80 % состоят из воды, подвергаются электролизу, образуя положительно и отрицательно заряженные ионы.
В области возле анода (положительного полюса) наблюдаются гидратация тканей и ионы водорода, сопровождающиеся повышением кислотности, и выделения газообразного кислорода и хлора. В области катода (отрицательный полюс) наблюдаются дегидратация тканей и гидроксильные ионы, сопровождающиеся понижением кислотности, и выделение газообразного водорода. Разность электрических потенциалов заставляет положительные ионы покидать опухоль и мигрировать к катоду. Электрохимическая картина происходящего напоминает процесс, происходящий в приборах для электроактивации воды; только здесь в качестве раствора используется местная тканевая жидкость.
Поток электронов, мигрирующий с катода вглубь ткани, образует анионы и нейтрализует катионы, создающие высокую кислотность во внеклеточном пространстве. Таким образом происходит местное снижение кислотности опухоли. Насыщение ткани катионами вблизи катода происходит за счёт их истощения в других тканях. Однако благодаря тому, что в здоровой ткани имеется гораздо лучшее движение жидкости по сравнению с опухолью, это истощение можно компенсировать приёмом растворов, содержащих катионные электролиты.
Одновременно с этим в область гликолитической опухоли можно транспортировать щелочные элементы, которые будут снижать внеклеточную кислотность. Продолжительность процедуры электрофореза – до 3-5 часов при плотности тока 0,15-0,3 мА/см2. Сеансы проводят на протяжении 6-12 недель в не-терапийный период. Единственным, но принципиальным минусом электрофореза является то, что проникновение действующих веществ под действием электрического поля ограничено несколькими миллиметрами.
Кислотно-щелочная модуляция имеет хорошую теоретическую базу; успешные доклинические испытания; невысокую стоимость, доступность, низкую токсичность и изученность терапевтических средств. Однако она требует постоянного контроля электролитного баланса, а также общей кислотности ткани, как минимум, по показателям кислотности мочи (краткосрочная реакция) и кислотности слюны (долгосрочная реакция). Преимущества данной терапии настолько очевидны, что трудно понять, почему нею до сих пор пренебрегают.
Электролиты – это химические вещества, которые регулируют важные физиологические функции организма. Это бикарбонат, натрий, хлориды, магний, калий, кальций, фосфаты. При растворении в воде электролиты образуют положительно и отрицательно заряженные ионы (соответственно, катионы и анионы), создавая электропроводную среду. Натрий, калий, магний, кальций образуют катионы, а сульфаты, нитраты, фосфаты, фториды и хлориды – анионы.
Здоровая биологическая среда клетки зависит, в первую очередь, от кислотно-щелочного баланса, минерального баланса, окислительно-восстановительного потенциала и проводимости, что определяется концентрацией различных электролитов в тканях организма.
Адекватное соотношение внеклеточных и внутриклеточных электролитов необходимо для сохранения клеточного объёма, а также для переноса сквозь клеточную мембрану некоторых веществ.
Дисбаланс в электролитах может повлиять на работу сердца *, нервной системы * и на клеточные функции *. Главным образом, это касается соотношения внутриклеточных электролитов (калий, магний) к внеклеточным электролитам (натрий, кальций). Например, при увеличении соотношения натрий:калий происходит задержка жидкости в организме.
Широкомасштабное клиническое исследование 2020 года обнаружило, что у 53 % пациенток с раком груди на момент госпитализации наблюдались кислотно-щелочной дисбаланс или, как минимум, одна электролитная аномалия *. Чаще всего недостающими минералами были магний (15 % всех случаев), кальций (12 %), фосфор (12 %), калий (11 %) и натрий (8 %); а избыточным был хлор (12 %). Конечно, это исследование не доказывает зависимости риска заболевания от дисбаланса электролитов, однако оно заставляет задуматься о широкой распространённости этой серьёзной проблемы.
Пациенты, получавшие противо
Баланс щелочных элементов (калия и натрия). Рацион современного человека содержит слишком малые объёмы растительной пищи, являющейся основным источником калия. Предполагается, что рацион человека палеолитического периода обеспечивал соотношение калий:натрий примерно 5:1 *. Адекватное соотношение поступления в организм калий:натрий составляет 3,5:1, и должно быть не ниже 1,5:1, в то время как современная диета имеет обратное соотношение *.
ВОЗ рекомендует ограничить потребление поваренной соли 5 граммами в день *, однако при широко распространённом низком потреблении калия из овощей следование этой рекомендации неизбежно приведёт к серьёзному дисбалансу калий:натрий. Рекомендуемое диетическое соотношение K:Na должно быть 5:1 или выше, а клеточное соотношение K:Na должно быть выше 10:1 *. У женщин с кистозной болезнью низкое соотношение K:Na внутри кист по сравнению с высоким соотношением K:Na ассоциируется с более высоким риском рака груди *.
Организм человека эволюционным путём генетически настроен на потребление большого количества калия из растительной пищи, поэтому легко теряет его с потом и мочой. С другой стороны, в современной пище слишком много натрия, поступающего с поваренной солью. И который организм старается удержать из-за отсутствия натрия в растительной пище. В результате, в организме создаются условия для избытка натрия и аномального соотношения калия к натрию.
Исходя из этого, легко заметить, что рассмотренная чуть выше защелачивающая терапия с использованием бикарбоната натрия неизбежно будет вызывать дисбаланс между между калием и натрием, если натрий не будет уравновешен соответствующим количеством калия, например в виде цитрата калия. Но даже без обращения к этой терапии, рацион современного человека создаёт настолько серьёзный дисбаланс калия и натрия, что заставляет серьёзно задуматься о приёме калия в виде добавок. А ещё лучше – об увеличении потребления растительной пищи.
Наиболее богаты калием такие пищевые источники, как банан, картофель, авокадо, а также сухофрукты – инжир, курага, финик, изюм, чернослив. С этой точки зрения, свежеотжатые соки, являются более полезным питьём, чем чистая вода, которая лишь выносит калий из организма. Имеются в виду овощные соки, богатые калием, а не фруктовые соки, богатые сахаром.
Баланс щелочноземельных элементов (магния и кальция). Кальций и магний являются химическими близнецами, но в то же время своего рода биохимическими антагонистами. В то время как магний способствует текучести крови и защищает от образования тромбов, ведущих к инфарктам и инсультам, кальций наоборот, способствует сгущению крови и предотвращению кровопотерь. В то время как кальций сокращает мышцы и возбуждает нервную систему, магний содействует их расслаблению. Магний проявляет анти-апоптотические свойства, в то время как кальций – про-апоптотические.
Мыши с лёгочной карциномой Льюиса, получавшие диету с дефицитом магния, значительно замедляли рост первичной опухоли (до 70 %). Однако в то же самое время дефицит магния увеличивал метастатический потенциал (на 22 %) *. Это свидетельствует о важности контроля за уровнем и соотношением обоих этих элементов.
Для женщин адекватное соотношение поступления в организм кальций:магний должно составлять примерно 2,5:1. При их оптимальном соотношении, кальций успешно усваивается и мигрирует из тканей в кости, укрепляя зубы и скелет. При дефиците магния в организме, кальций покидает кости и замещает магний в тканях. Это не только ослабляет зубы и кости – кальций в виде фосфатов, оксалатов и солей других органических кислот откладывается в органах и на стенках сосудов. В результате повышается риск артроза, инсульта, инфаркта, сердечно-сосудистых заболеваний, аритмии, гипертонии, камней в почках и жёлчном пузыре. Минерализуется также опухолевая зона молочной железы, что способствует продвижению рака *.