Gezondheidsstrategie.
Alle voorgaande punten bieden een achtergrond die gunstig is voor de gezondheid van de borsten. Het is noodzakelijk, maar mogelijk geen voldoende voorwaarde om de groei, invasie en metastase van een reeds gevormde tumor te remmen. Hieronder zullen we manipulaties bekijken die rechtstreeks op de tumor zijn gericht.
Het vernietigen van kankercellen staat centraal in de moderne oncologie. De huidige zorgstandaard voor borstkanker omvat chirurgie, bestraling en chemotherapie, zoals cisplatine, paclitaxel, carboplatine, bevacizumab, doxorubicine, cyclofosfamide, docetaxel en epirubicine *.
Veel natuurlijke stoffen die niet in het behandelingsprotocol zijn opgenomen, kunnen op zichzelf het effect van chemotherapie versterken of kankercellen vernietigen. Sommigen van hen worden gebruikt in verschillende klinieken voor complementaire of alternatieve geneeswijzen. Hoewel ze mogelijk veel mildere bijwerkingen hebben, is het onwaarschijnlijk dat ze effectiever zijn dan klinisch gebruikte middelen *.
Vitamine C, toegediend in hoge doses intraveneuze infusies, is een van de remedies die lange tijd door de orthodoxe geneeskunde worden genegeerd. Therapie met deze natuurlijke, niet-giftige en goedkope stof kan nuttig zijn bij de behandeling van hardnekkige tumoren * zonder de bijwerkingen die kenmerkend zijn voor traditionele chemotherapie.
Vitamine C vertoont in lage doses een antioxiderende werking, maar is in hoge doses juist pro-oxidant *. Het creëren van een hoge concentratie vitamine C houdt echter verband met het probleem van de introductie ervan in het lichaam. Orale inname van zelfs de maximaal getolereerde dosis (18 g) vitamine C kan de plasmaconcentratie niet hoger dan 220 μM doen stijgen, terwijl deze door intraveneuze toediening kan worden verhoogd tot 26 mM * *. Dergelijke hoge niveaus van vitamine C produceren enorme hoeveelheden waterstofperoxide in de intercellulaire ruimte en in de cellen, een sterk oxidatiemiddel dat in vitro selectief cytotoxisch is voor kankercellen * * * *.
Kankercellen zijn gevoeliger voor oxidatieve stress omdat ze al overladen zijn met oxidanten. Bovendien produceert vitamine C op een andere manier vrije radicalen: door metaalionen zoals koper of ijzer te verminderen (Fenton-reactie). En omdat de concentratie ijzer in kankercellen toeneemt, wordt de oxidatieve stress voor hen verder vergroot.
Vitamine C beschadigt selectief kankercellen vanwege hun verhoogde consumptie van glucose. Door de actieve opname van glucose neemt het aantal en de activiteit van glucosetransporters in glycolytische cellen sterk toe. Het is bekend dat vitamine C door dezelfde transporters naar de cel wordt getransporteerd als glucose * * *, en daarom is de consumptie van vitamine C door glycolytische cellen meerdere malen actiever dan de consumptie door normale cellen.
Hoewel ascorbaat alleen een aanzienlijk zwakker remmend effect heeft op de tumorgroei vergeleken met chemotherapie, laten sommige klinische onderzoeken een aanzienlijk voordeel zien bij het combineren van ascorbaat met bestralings- * en chemotherapie *. In de zure, metaalionenrijke omgeving van een tumor werkt ascorbaat op dezelfde manier als ioniserende straling, waarbij cellen worden gedood door DNA-schade door vrije radicalen. Een hoge dosis ascorbaat put de intracellulaire voorraden antioxidanten uit, zodat het ook effectief kan worden gecombineerd met andere therapieën die zijn gebaseerd op toenemende oxidatieve stress.
Het kan echter de bijwerkingen van chemotherapie * verminderen en de overlevingskans van de patiënt vergroten *. Bovendien verminderde ascorbaat in dierstudies de daling van het aantal witte bloedcellen, het gewichtsverlies, de hepatotoxiciteit en de cardiomyopathie, en verlichtte het ook vele andere bijwerkingen veroorzaakt door chemotherapie * * * *.
De antitumorale eigenschappen van vitamine C zijn niet beperkt tot het cytotoxische effect ervan. Sommige in vitro onderzoeken hebben aangetoond dat hoge doses ascorbinezuur, vooral in combinatie met selenium, ervoor zorgen dat cellen in een precancereuze toestand terugkeren naar een normaal metabolisme * * *; uiteraard als gevolg van de onderdrukking van de anaërobe ademhaling *, en onderdrukt ook de angiogenese * en bevordert de celdifferentiatie *.
Om verzuring van het bloed veroorzaakt door ascorbinezuur te voorkomen, wordt aanbevolen om de zouten ervan (ascorbaten), zoals natriumascorbaat, of, nog beter, kaliumascorbaat, te gebruiken voor intraveneuze infusies.
Er bestaat geen goedgekeurd protocol voor het klinische gebruik van deze therapie, maar sommige klinieken voor alternatieve behandeling gebruiken het Riordan-protocol * *.
De huidige aanbevelingen omvatten het volgende: de dosering van ascorbaat moet ongeveer 1 g/kg zijn; de toedieningsfrequentie moet minimaal 2 infusies per week zijn. De duur van de therapie is ongeveer 3 maanden, waarna het mogelijk is om de effectiviteit ervan te evalueren *.
In één klinische studie *, bij een infusiesnelheid van 0,5 g/min, was de aanvangsdosering voor de eerste 2 sessies 15 g vitamine C met een passende hoeveelheid draagvloeistof. Voor de 3e en 4e sessie – 25 g vitamine C en 200 mg magnesiumchloride om vasculaire spasmen te voorkomen. Voor de 5e en 6e sessies – 50 g vitamine C en 200 mg magnesiumchloride. Voor alle volgende sessies – 75 g vitamine C plus een passende hoeveelheid draagvloeistof en 200 mg magnesiumchloride. Voor patiënten met extreem agressieve tumoren werd de dosering verhoogd tot 100 g vitamine C en 400 mg magnesiumchloride. De beoogde plasma-vitamine C-concentratie was ongeveer 350 tot 450 mg/dl. De behandelingskuur bestond uit 21 dagen dagelijkse intraveneuze infusies, gevolgd door infusies elke 2-3 dagen per week, totdat het uiteindelijke effect werd bereikt. Daarnaast werden de additieven gebruikt die hieronder (drie paragrafen later) worden vermeld.
In deze studie werd bij drie van de vier patiënten met ER+-borstkanker die zich aan het behandelingsprotocol hielden, de primaire tumor in stadium II binnen drie weken behandeling teruggebracht tot de helft van de initiële meting, en twee van deze drie patiënten ondervonden vervolgens een volledige regressie.
Ascorbaat wordt zeer snel gemetaboliseerd en de spiegels dalen aanzienlijk binnen 2 uur na toediening. Daarom zou een effectievere methode zijn om 60 gram ascorbaat (in 500 ml water voor injectie) gedurende 60 minuten in een ader te injecteren, en vervolgens nog eens 60 gram langzaam en continu te injecteren gedurende de volgende 6 uur. Deze oplossing zal het mogelijk maken, zonder plotselinge sprongen in de concentratie van ascorbaat, een langere verzadiging van het plasma ermee te bereiken op een redelijk effectief cytotoxisch niveau *. Continue, constante infusies kunnen de effectieve therapeutische dosering van vitamine C verder verlagen – tot 20 g/dag *.
De toevoeging van liponzuur aan ascorbaat in een verhouding van 1:10 maakte De toevoeging van liponzuur aan ascorbaat in een verhouding van 1:10 maakte in vitro een zesvoudige reductie mogelijk van de dodelijke dosis (LC50) voor kankercellen, tenminste voor rectale kankercellen. Andere boosters voor de effectiviteit van hooggedoseerd ascorbaat zijn vitamine К3 *, co-enzym Q10, acetyl-L-carnitine, magnesium, aspartaat, vitamine B-complex en laaggedoseerde kopersupplementen *. Essentieel is het hoge zuurstofgehalte in het bloed, waaruit vitamine C vrije radicalen aanmaakt. Er mag dus een verhoogd effect worden verwacht als deze therapie wordt gecombineerd met hyperbare zuurstoftherapie.
Andere opties om de effectiviteit van vitamine C-therapie te verbeteren *:
- een dieet met weinig suiker, koolhydraten en vlees en veel verse groenten en fruit;
- supplementen voor de gezondheid van het maagdarmkanaal: pancreasenzymen (400-1'200 mg/dag), probiotica (9×109 eenheden/dag);
- antioxidantsupplementen: α-liponzuur (600-1'200 mg/dag), niacine (500-1'500 mg/dag), resveratrol (10-20 mg/kg/dag);
- algemene versterkende supplementen: CoQ10 (150-300 mg/dag), cobalamine (80-100 mg/dag), foliumzuur (0,5-1 mg/dag), thiamine (5-30 mg/dag);
- immuunsupplementen: vitamine D3 (5'000-10'000 IE/dag), vitamine E (0,05 mg/dag), selenium (200 μg/dag), zink (50 mg/dag), β-glucaan (100-200 mg/dag);
- ontstekingsremmende supplementen: curcumine (1-3 g/dag), lijnzaadolie (3-6 g/dag), quercetine (0,5-1 g/dag), boswellia (1,2-2,4 g/dag), silymarine (300-900 mg/dag).
Een contra-indicatie voor behandeling met ascorbaat is een tekort aan het enzym glucose-6-fosfaatdehydrogenase (G6PD), dat voorkomt bij 0,5% van de bevolking. Significante negatieve bijwerkingen van langdurige hoge doses vitamine C zijn onder meer: verhoogde bloedstolling; mogelijk tekort aan vitamine B12, foliumzuur, koper en ijzer; remming van de pancreas; verhoogde bloeddruk; verminderde nierfunctie en mogelijke groei van nierstenen.
De vraag naar de mogelijkheid dat kankercellen resistentie tegen geneesmiddelen tegen ascorbaat verwerven, blijft open. Een ander moeilijk probleem is de algehele buitensporige toename van de hoeveelheid vrije radicalen die door ascorbaat in het lichaam worden geproduceerd. Omdat de selectiviteit ervan alleen gebaseerd is op de hogere opname ervan door kankercellen, kan een hoge dosis ascorbaat potentieel giftig zijn voor normale lichaamscellen die de neiging hebben grote hoeveelheden glucose te consumeren. Lokale toediening van ascorbaat zou dit probleem kunnen verlichten, maar deze toedieningsweg is nog niet gerapporteerd.
Infusietherapie met hoge doses ascorbaat is alleen beschikbaar in een klinische setting onder begeleiding van gekwalificeerd personeel en wordt alleen gebruikt in alternatieve of aanvullende behandelingsklinieken. Als monotherapie is ascorbaat geen geneesmiddel voor kanker, maar als onderdeel van een uitgebreid behandelprogramma verbetert ascorbaat de levenskwaliteit van kankerpatiënten en vergroot het hun overlevingskansen.
Het probleem dat het wijdverbreide gebruik ervan tegenhoudt, is het ontbreken van een betrouwbare, positieve bewijsbasis verkregen uit uitgebreide klinische onderzoeken. Maar dit is een veel voorkomend probleem bij het op de markt komen van alle eenvoudige, goedkope en duidelijk niet-patenteerbare medicijnen. Onder individuen en organisaties zijn er geen mensen die bereid zijn miljarden dollars aan onderzoek uit te geven zonder de hoop op een overeenkomstige winst, en regeringen geven er de voorkeur aan om geld aan andere doeleinden te besteden.
Amygdalin, aanwezig in de pitten van steenvruchten, is een bekend complementair medicijn. Hij werd algemeen bekend dankzij een schandalig verhaal toen de farmaceutische industrie, bang voor mogelijke winstderving, de medische wetenschap in gevaar bracht.
Net als ascorbaat gebruikt amygdaline hun toegenomen honger naar glucose om kankercellen selectief te doden. Naast oxidatieve wapens gebruikt hij echter ook giftige wapens.
Het amygdalinemolecuul bevat twee glucosemoleculen, waardoor het gemakkelijk in de cel kan worden getransporteerd, waar het als gevolg van metabolisatie wordt afgebroken tot moleculen glucose, benzaldehyde en het CN-ion van blauwzuur. De laatste twee moleculen zijn cellulaire toxines. Cyanide blokkeert, door zich te binden aan het ademhalingsenzym cytochroomoxidase, de mitochondriale ademhaling van de cel, terwijl benzaldehyde de glycolytische ademhaling blokkeert *.
In aanwezigheid van zuurstof wordt benzaldehyde geoxideerd tot benzoëzuur, dat vervolgens via de nieren wordt geëlimineerd. Onder hypoxische omstandigheden die in de tumor worden waargenomen, blijft benzaldehyde echter niet-geoxideerd en hoopt het zich op. Hoewel het voor een cyanidemolecuul vanwege zijn kleine omvang gemakkelijk is om een cel te verlaten, is het voor benzaldehyde moeilijker om dit te doen. Als we tegelijkertijd ook de activiteit onderdrukken van membraanpompen die gifstoffen uit de cel pompen, dan zal de toxische werking van benzaldehyde blijkbaar toenemen.
Door de oxidatieve stress veroorzaakt door amygdaline *, maar ook door een toename van de verhouding tussen pro-apoptotische en anti-apoptotische eiwitten, sterven borstkankercellen, ongeacht hun hormoongevoeligheid, door apoptose *.
Klinische onderzoeken tonen aan dat amygdaline ook ontstekingsremmende * en pijnstillende * effecten heeft. Bovendien stimuleert het het immuunsysteem *. Resultaten uit in vitro- en laboratoriumonderzoek bij muizen hebben het potentiële voordeel van amygdaline tegen tumormetastasen aangetoond *.
De tweede fase van de klinische proef, uitgevoerd in Mexico, omvatte 1'200 patiënten met gevorderde maligniteiten die werden behandeld met amygdaline in verschillende doseringen. Intraveneuze infusies van 6-9 g amygdaline gedurende 20 minuten lieten een antitumoreffect zien. Volledige remissies, gedeeltelijke verlichting en langdurige stabilisatie werden waargenomen bij bijna 33% van de patiënten, die in meer dan 70% van de gevallen niet langer in aanmerking kwamen voor traditionele behandeling. In meer dan 45% van de gevallen werden subjectieve verbeteringen waargenomen: verbetering van de algemene toestand van de patiënt, verbetering van de eetlust en vermindering van pijn. Bijna alle patiënten konden morfinederivaten vervangen door niet-narcotische pijnstillers in minder dan vier weken na het starten met amygdaline *. Dit werk is echter niet gepubliceerd in peer-reviewed tijdschriften.
Zelfs als dergelijke resultaten zouden worden overschat, kan amygdalinetherapie de patiënt helpen de ontberingen van de ziekte te doorstaan en het effect van andere therapieën versterken. Amygdalin biedt geen langetermijneffecten en vereist daarom constant gebruik. Op zichzelf levert het geen sterke effecten op in termen van het remmen van de tumorgroei, en is het niet in staat tot regressie ervan te leiden.
De combinatie van amygdaline met andere geneesmiddelen kan het antitumoreffect versterken. Zo'n versterker zou de volgende combinatie kunnen zijn:
- een complex van pancreasenzymen, zoals Wobenzym™ (3 tabletten twee uur na elke maaltijd);
- vitamine A (1 mg/dag), C (100 mg/dag), D (50 μg/dag), E (15 mg/dag);
- zink, selenium en jodium;
- omega-3 vetzuren;
- methylsulfonylmethaan;
- plantaardige antioxidanten en kruiden;
- vers geperste groentesappen.
Net als in het geval van vitamine C is een ernstig nadeel van deze therapie de noodzaak om amygdaline toe te dienen via intraveneuze infusies, omdat het oraal innemen van amygdaline leidt tot de afbraak van het molecuul al in de zure omgeving van de maag en vervolgens in de darmen. Als gevolg hiervan komt cyanide in de algemene bloedbaan terecht en vergiftigt het het hele lichaam, in plaats van de kankercellen binnen te dringen en alleen deze te vergiftigen. Dit verklaart de paradox dat hoewel injectie van 6-9 gram amygdaline veilig een therapeutisch effect oplevert, orale toediening van slechts 3 gram amygdaline ernstige cyanidevergiftiging kan veroorzaken *.
Mogelijke bijwerkingen van amygdalinetherapie zijn onder meer een lichte maar scherpe daling van de bloeddruk, een toename van hemoglobine en het aantal rode bloedcellen. Bij een aanzienlijke overdosis verschijnen symptomen van cyanidevergiftiging: griepachtige toestand, bloeddrukdaling, koorts, duizeligheid, jeuk, zwakte, misselijkheid en in ernstige gevallen de dood.
In de literatuur zijn geïsoleerde gevallen beschreven van een positieve respons op behandeling met amygdaline. Zelfs in de onderzoeken waarin amygdaline en zijn analogen als ineffectief werden beschouwd, was er in ongeveer een kwart van de gevallen sprake van een verbetering van de levenskwaliteit van patiënten. Tegelijkertijd ondervonden velen van hen bijwerkingen en symptomen van cyanidevergiftiging *.
Net als bij vitamine C is de wetenschappelijke basis voor de voordelen van amygdaline bij borstkanker nog steeds erg zwak *. Er zijn geen grote, overtuigende klinische onderzoeken gepubliceerd *. De selectiviteit van zijn werking tegen kankercellen, zoals vitamine C, is laag. En vergeleken met vitamine C lijkt amygdaline subjectief een minder effectieve therapie te zijn. Bovendien wordt het therapeutische amygdaline (merknaam Laetrile™) voornamelijk in Mexico vervaardigd en kan het moeilijk verkrijgbaar zijn.
Artemisinine, aanwezig in jaarlijkse alsem, veroorzaakt ook de dood van kankercellen door de concentratie van oxidatiemiddelen te verhogen. Maar in tegenstelling tot vitamine C en amygdaline veroorzaakt artemisinine de dood van kankercellen, niet alleen door apoptose of necrose, maar ook door de zogenaamde ferropoptose *.
In kankercellen, vooral in de lysosomen, bevindt zich een abnormaal hoog ijzergehalte, dat de cellen nodig hebben voor het delingsproces. Door te reageren met ijzer vormt artemisinine in grote hoeveelheden verschillende vormen van vrije radicalen die eiwitmoleculen vernietigen, waaronder lysosoommembranen. De doorbraak van de agressieve inhoud van lysosomen in het cytosol van de cel veroorzaakt catastrofale vernietiging binnenin de cel, wat leidt tot celdood *.
De specifieke aard van de productie van vrije radicalen door artemisinine maakt het mogelijk om het te combineren met andere therapieën als aanvullende behandeling *. Uit preklinische onderzoeken blijkt dat artemisinine alleen schadelijke effecten heeft op tumorcellen en niet op immuuncellen *. Helaas is artemisinine slecht oplosbaar in water en vet, heeft het een lage orale biologische beschikbaarheid en een korte halfwaardetijd. Andere nadelen zijn de bijwerkingen, waaronder neurotoxiciteit, brachycardie, verlaagde hemoglobinewaarden en andere.
Er zijn verschillende synthetische en semi-synthetische artemisinepreparaten ontwikkeld die deze nadelen grotendeels missen, maar het klinische bewijs van hun effectiviteit is nog steeds erg zwak. Enkele rapporten van klinische onderzoeken met artemisineverbindingen hebben nog geen hoge resultaten opgeleverd * * *. Tot nu toe zijn er geen meldingen geweest van omkering van het tumorproces onder invloed van artemisinemedicijnen.
Salinomycine is een ionofoor antibioticum dat wordt gebruikt voor de behandeling van coccidiose bij pluimvee. Salinomycine wordt beschouwd als een potentieel veelbelovend antitumormiddel *, maar er zijn nog niet voldoende overtuigende gegevens om het aan te bevelen voor klinische goedkeuring.
Salinomycine vertoont in vitro op verschillende manieren cytotoxische effecten. Ten eerste creëert het oxidatieve stress in de cellen door de productie van reactieve zuurstofsoorten (ROS), wat leidt tot een verminderde mitochondriale functie en daaropvolgende apoptose * *. Ten tweede activeert het de stress in het endoplasmatisch reticulum van de cellen, wat de dood van kankercellen veroorzaakt door autofagie *. Beide acties kunnen elkaar echter verzwakken. Autofagie verzwakt apoptose veroorzaakt door ROS-productie, waardoor kankercellen worden beschermd * *.
Salinomycine is een krachtige remmer van P-glycoproteïne *, die cellen ongevoelig maakt voor chemotherapie door gifstoffen actief uit de cel te verwijderen. Bovendien kan salinomycine deze taak effectiever aan dan verapamil *.
Terwijl veelgebruikte chemotherapiemedicijnen zich richten op kankercellen in de tumormassa, doodt salinomycine selectief * borstkankerstamcellen *, evenals multiresistente * en apoptotisch-resistente * kankercellen. De bijzondere waarde van salinomycine is dat het effectief is tegen triple-negatieve borstkankerstamcellen * *. De combinatie van salinomycine met traditionele therapie lijkt dus veelbelovend, wat het risico op herhaling van de ziekte zou kunnen verminderen.
De combinatie van salinomycine en vrijwel alle standaard cytotoxische geneesmiddelen versterkt hun effect, zij het in verschillende mate van ernst *. De combinatie van salinomycine met trastuzumab (een monoklonaal antilichaam tegen HER2) werkt ook synergetisch *. Salinomycine verhoogt de gevoeligheid van luminale type A-kankercellen voor tamoxifen, waardoor wordt voorkomen dat ze resistentie tegen geneesmiddelen ontwikkelen * *. Bovendien verhoogt salinomycine de gevoeligheid van kankercellen, niet alleen voor chemotherapie, maar ook voor bestralingstherapie *.
In muismodellen verminderden intraperitoneale injecties van salinomycine (2,5 mg/kg) de groei van de geïmplanteerde tumor met een orde van grootte *, wat apoptose, necrose en differentiatie van epitheelkankercellen veroorzaakte, vergeleken met controles. Dagelijkse intraperitoneale injecties van salinomycine (5 mg/kg) of paclitaxel (5 mg/kg) gedurende 5 weken bij met borsttumor geënte muizen (SUM159) vertraagden de vorming van voelbare tumor met 2 weken vergeleken met controledieren. Na vier weken behandeling was het aantal cellen dat mammosferen vormde in de salinomycinegroep half zo hoog. Hier leidde paclitaxel tot een tweevoudige toename van de vorming van metastasen, terwijl salinomycine juist tot een viervoudige afname leidde *. Omdat mammosferen voornamelijk bestaan uit kankerstamcellen *, suggereert dit effect dat salinomycine in staat is deze te doden.
Bij patiënten met gemetastaseerde borst-, eierstok- en hoofd- en nekkanker resulteerde intraveneus salinomycine in een gedeeltelijke regressie van de tumormetastase met weinig acute en langdurige bijwerkingen *. Hier werd salinomycine (200-250 μg/kg om de dag gedurende drie weken) alleen of in combinatie met erlotinib toegediend, waardoor het effect van laatstgenoemde werd versterkt. Maar dit lijkt tot nu toe het enige klinische onderzoek naar salinomycine te zijn, uitgevoerd in 2012.
Salinomycine is echter zeer giftig en kan schadelijke effecten hebben op zenuwcellen en normale stamcellen, waardoor het klinische gebruik ervan wordt beperkt. Acute vergiftiging bij mensen kan worden veroorzaakt door een dosering van 1 mg/kg *. Typische symptomen zijn kortademigheid, duizeligheid, misselijkheid, zwakte in de benen, fotofobie en hoge bloeddruk *. Zelfs bij zeer lage concentraties salinomycine kan echter een verergering van de gevoeligheid van kankercellen voor antimitotische geneesmiddelen worden bereikt, waardoor het mogelijk wordt doses salinomycine te combineren met chemotherapie die de patiënt kan verdragen.
Onderdrukking van de proliferatie. Terwijl cytotoxinen kankercellen direct doden, voorkomen antimitotische middelen dat ze zich delen door de celcyclus te vertragen. Antimitotische middelen kunnen verschillende effecten hebben op tubuline * en inwerken in verschillende stadia van de celcyclus *.
Antimitotische kruidengeneesmiddelen worden, net als standaard chemotherapiemedicijnen, gebruikt voor snelle tumorgroei en niet langer dan 1,5 maand. Tijdens chemotherapie worden alle bovenstaande punten van het programma †, behalve het dieet en de algemene toon, geannuleerd. Vrouwen in de vruchtbare leeftijd moeten effectieve methoden gebruiken om zwangerschap te voorkomen, minstens een maand voordat ze met een chemotherapiekuur beginnen, maar ook tijdens de kuur en gedurende een maand na voltooiing ervan.
Van heel veel natuurlijke stoffen is bekend dat ze een antimitotisch effect hebben *, hoewel veel zwakker dan standaard chemotherapiemedicijnen, inclusief geneesmiddelen die zijn ontwikkeld op basis van plantaardige stoffen. Het bewijs voor hun antimitotische activiteit is echter grotendeels gebaseerd op in vitro-onderzoeken, en slechts enkele zijn in klinische omgevingen getest.
Hormoononafhankelijke borstkankercellen (MDA-MB-231). Van de 897 in vitro ethanolextracten van natuurlijke producten die werden getest *, vertoonden er 14 een toxiciteitsonafhankelijke groeiremming van 50% (IG50) bij concentraties lager dan 30 μg/ml, waarvan slechts de volgende 7 beschikbaar zijn *:
Mandrake (Podophyllum peltatum), wortel, (IG50<1 μg/ml);
Westerse levensboom (Thuja occidentalis), twijgen met bladeren (IG50=4,4 μg/ml);
Maretak (Viscum album), bladeren (IG50=9,6 μg/ml);
Speranskia (Speranskia tuberculata), kruid (IG50=14,0 μg/ml);
Bentonietklei (Bentonite clay) (IG50=14,7 μg/ml);
Meekrap (Rubia tinctorum), wortel (IG50=20,5 μg/ml);
Griekse alant (Inula helenium), wortel (IG50=28,8 μg/ml).
Andere beschikbare extracten zijn minder effectief:
Terminalia (Terminalia arjuna), stengelschors (IG50=40,8 μg/ml);
Granaatappel (Punica granatum), fruit (IG50=41,0 μg/ml);
Jeneverbes (Juniper Communus), bessen (IG50=42,0 μg/ml);
Boswellia (Boswellia carterii), harsachtige wierook (IG50=58,8 μg/ml);
Eucalyptus (Eucalyptus globulus), bladeren (IG50=59,0 μg/ml);
Phyllanthus (Phyllanthus niruri), bladeren (IG50=59,6 μg/ml),
Wilde geranium (Geranium maculatum), wortel (IG50=60,2 μg/ml);
Rhodiola (Rhodiola kirilowii), wortel (IG50=64,7 μg/ml);
Chimaphila (Chimaphila umbellata), bovengronds deel (IG50=66,2 μg/ml);
Kruidnagel (Syzygium aromaticum), bloemknoppen (IG50=68,3 μg/ml);
Houttuynia (Houttuynia cordata), wortel (IG50=72,1 μg/ml);
Japanse duizendknoop (Polygonum cuspidatum), wortel (IG50=73,4 μg/ml);
Zwarte braam (Rubus fruticosus), fruit (IG50=74,3 μg/ml);
Indiase meekrap (Rubia cordifolia), wortel (IG50=76,6 μg/ml);
Neem (Azadirachta indica), bladeren (IG50=79,4 μg/ml);
Moederkruid (Tanacetum parthenium), bloemen (IG50=80,1 μg/ml).
Er werden extracten bereid in een hoeveelheid van 5 g droog poeder van het oorspronkelijke product per 100 ml absolute ethanol.
Sommige plantenextracten in vitro zijn in staat de deling van tumorcellen te stoppen, uitsluitend vanwege hun hoge toxiciteit:
Wilde yam (Dioscorea villosa), wortel, (IG50=0,1 μg/ml);
Trilliumslinger (Trillium pendulum), wortel (IG50=1,1 μg/ml);
Parelzaad (Lithospermum canescens), wortel (IG50=4,6 μg/ml);
Drakenbloedboom (Dracaena draco, Croton draco, Croton lechleri), blad- en schorspigment (IG50=12 μg/ml);
Kalmoes (Acorus calamus), wortel (IC50= 13,7 μg/ml *).
Van deze vijf planten zijn alleen de eerste en de laatste beschikbaar.
Preklinische onderzoeken tonen ook apoptotische, antiproliferatieve en antimetastatische effecten aan van de volgende planten:
Sophora (Sophora flavescens), wortel * * *;
Ginkgo biloba (Ginkgo biloba), bladeren * *;
Goudzegel (Hydrastis canadensis), hele plant, wortel *;
Aloë (Aloe vera), bladeren * *.
Hormoonafhankelijke borstkankercellen (MCF-7). Van de 76 bestudeerde chloroform-ethanol plantenextracten werd het hoogste antiproliferatieve effect in vitro aangetoond door:
Alant (Inula graveolens), wortel (IC50=3,833 μg/ml),
Dominicaanse salie (Salvia dominica), bladeren (IC50=7,28 μg/ml),
Canadese fijnstraal (Conyza canadensis), wortel (IC50=12,76 μg/ml),
Duizendblad (Achillea santolina), bloemen (IC50=24,12 μg/ml) *.
Andere antiproliferatieve planten:
Evaluatie van geneeskrachtige plantenextracten * die in de traditionele Indiase geneeskunde worden gebruikt voor de behandeling van kanker toonde significante antioxiderende en antiproliferatieve activiteit aan van 10 daarvan (in afnemende volgorde van activiteit): (Asclepias curassavica) ⇒(Cynodon dactylon) ⇒(Costus speciosus) root ⇒(Amaranthus tricolor) ⇒ (Merremia emerginata) ⇒ (Ophiorrhiza mungos) ⇒ (Tabernaemontana heyneana) ⇒ (Blepharis maderaspatensis) ⇒ (Aegle marmelos) ⇒ (Achyranthes aspera). Rode amarant (Amaranthus paniculatus) of Driekleurige amarant (Amaranthus tricolor), wijd verspreid in Europa. Ethylacetaatextract van amarantbladeren had een IC50 van 19,21 μg/ml voor de kankercellijn MCF-7 versus 39,44 μg/ml voor de niet-kankercellijn VERO na 72 uur in vitro behandeling.
In een ander in vitro onderzoek onderdrukten meer dan 150 traditionele kruiden geassocieerd met oestrogene effecten de groei van ER– -borstkankercellen door Mandrake (Podophyllum peltatum), Sanguinaria (Sanguinaria canadensis), Juniper (Juniperus communis) en Maretak (Viscum album) aanzienlijk *.
Vanwege de slechte kennis, de ontoegankelijkheid, de moeilijkheid van normalisatie en assimilatie, problemen met de levering aan het doel, de snelle verwijdering uit het lichaam en de willekeurige werking van de actieve stoffen van deze planten, zijn slechts enkele uit deze hele lijst van praktisch belang *.
• Maretak (Viscum album).
De antitumoractiviteit van maretak in vitro is aangetoond via verschillende mechanismen: inductie van apoptose en necrose, remming van de celcyclus *
en activering van specifieke en niet-specifieke immuunsystemen *.
De combinatie van maretakbladextract met trastuzumab versterkte het in vitro antikankereffect van laatstgenoemde tegen de HER2+-borstkankercellijn (SK-BR-3) *.
Een soortgelijk synergetisch effect onderdrukt de proliferatie van zowel ER+ (MCF-7) als ER– (MDA-MB-231) cellijnen *.
Verschillende klinische onderzoeken bij borstkankerpatiënten die chemotherapie met maretak kregen, rapporteerden verbeteringen in overleving, tumorgrootte, remissie, kwaliteit van leven en een vermindering van bijwerkingen van chemotherapie * * *.
De veiligheid en werkzaamheid van maretak zijn vastgesteld in een klinisch onderzoek in meerdere centra *.
• Wilde yam (Dioscorea villosa).
In vitro-onderzoeken hebben een sterk kankerbestrijdend effect aangetoond van het ethylextract van wilde yamwortel en de verschillende componenten ervan *. Het extract vermindert de levensvatbaarheid van ER+ (MCF-7) en ER– (MDA-MB-231) kankercellen aanzienlijk bij een concentratie van 50 μg/ml als gevolg van verhoogde DNA-methylatie *.
Dioscin oefent zijn effect uit via de regulatie van een groot aantal genen *.
In aanwezigheid van 5,76 μM dioscine werd de invasie van TNBC-cellen (MDA-MB-231) met 65% verminderd *.
Dioscorealide B vertoonde een cytotoxisch effect tegen MCF-7 (IC50=2,76 μM) en MDA-MB-468 (IC50=9,93 μM) cellen *.
Diosgenine, een steroïde sapogenine dat als fyto-oestrogeen wordt beschouwd, veroorzaakt een duidelijke remming van de migratie van MDA-MB-231-cellen *
en onderdrukt de expressie van vetzuursynthase in HER2-cellen *.
Diosgenine kan in vitro de CSC-stameigenschappen effectief remmen en apoptose induceren in ER+ (MCF-7, T47D) en ER– (MDA-MB-231) borstkankercellen *.
Omdat diosgenine een hydrofobe stof is, produceren vetoplossingen van diosgenine hogere en persistentere niveaus in plasma vergeleken met een waterige oplossing. In een klinische studie bij gezonde vrijwilligers was de orale dosis 50 mg/dag yamextract in olijfolie-oplossing, overeenkomend met 8 mg/dag diosgenine, of 2'000 mg/dag gedroogde yamwortel *.
De cognitieve functie werd verbeterd als gevolg van het gebruik van diosgeninesupplementen.
Ondertussen geeft het gebruik van extract van hele yamwortel voor borstkanker nog steeds aanleiding tot enige bezorgdheid vanwege de mogelijke oestrogene effecten, en vereist aanvullend klinisch onderzoek.
Uit één onderzoek bleek dat suppletie met wilde yam de oestradiolspiegels in het speeksel consistent zeer laag hield, wat erop kan wijzen dat deze plant de oestradiolsynthese kan remmen *.
In een ander onderzoek verhoogden postmenopauzale vrouwen die rijst vervingen door 390 g/dag yam (Dioscorea alata) in hun dieet de serum-oestronconcentraties met 26% gedurende 30 dagen; geslachtshormoonbindend globuline (SHBG) – met 9,5% en estradiol – met 27% *.
• Ashwaganda (Withania somnifera).
De plant bevat withaferine A, dat bij ERα-positieve tumoren (MCF-7 en T47D) in vitro (bij 2,5 μM) cytotoxische werkzaamheid vertoont vergelijkbaar met doxorubicine *. Muizen die werden behandeld met intraperitoneale injecties van withaferine (4 mg/kg) hadden een significante vermindering in de ontwikkeling van zowel ER+ als ER–-gevestigde tumoren *. De dagelijkse dosis withaferine die overeenkomt met een persoon is 25 mg.
• Griekse alant (Inula helenium).
Bevat een rijke reeks sesquiterpenoïden. Sesquiterpeenlactonen onderdrukken in vitro de expressie van STAT3-doelgenen, waaronder cycline D1, c-myc en bcl-2, en induceren caspase-gemedieerde apoptose *.Isoalantolacton (20 μM) remt in vitro de adhesie, migratie en invasie van ER–cellen (MDA-MB-231) *.
• Salie (Salvia).
Ethanolextracten van Salvia syriaca, Salvia fruticosa en Salvia horminum vertoonden in vitro selectieve antiproliferatieve activiteit tegen ER+ borstkankercellijnen (MCF-7) met minimale toxiciteit tegen normale fibroblasten *, en extracten van Salvia triloba en Salvia dominica ook tegen ER+-cellen (T47D) *. Chinese salie Salvia miltiorrhiza vertoont sterke antiproliferatie-effecten op ER+-cellen (MCF-7), waardoor de celcyclus in de G1-fase tot stilstand komt via Akt- en p27-mechanismen *.
Tanshinone IIA, een actieve ingrediënt van salie, remt in vitro de proliferatie en veroorzaakt apoptose van kankercellen door de onderdrukking van meerdere genen die betrokken zijn bij de regulatie van de celcyclus, proliferatie, celapoptose en DNA-synthese. Bij behandeling met tanshinon werd de proliferatie van borstkankercellen significant geremd (IC50=0,25 μg/ml). Bovendien nam het aantal apoptotische zowel ER+ als ER– cellen toe, terwijl tamoxifen alleen ER+ cellen remde *. Tanshinone vermindert de expressie van ABC-transporters, waaronder P-gp, BCRP en MRP1, die chemotherapiemedicijnen uit de cel pompen *. Na behandeling met tanshinon waren de celproliferatie en de mammosfeervorming van CSC's aanzienlijk verminderd; en de tumorhoogte en het gemiddelde gewicht waren significant verminderd. Tanshinon heeft het potentieel om CSC’s te doden en kan hun groei zowel in vitro als in vivo remmen *.
• Zoethout (Glycyrrhiza glabra).
Glabridine, een van de componenten van zoethoutwortel, verzwakt de tumorgroei, invasie, migratie en CSC-achtige eigenschappen van ER–-muizenborsttumoren (MDA-MB-231) * *. Een ethanolisch extract van het flavonoïdencomplex van zoethoutwortel (100 mg/kg) halveerde de gewichtsgroei van borstkliertumoren die waren ingeënt bij muizen met ER–-tumoren (MDA-MB-231) met onderdrukking van ontstekingen, blokkeerde iNOS-expressie en inactivatie van de protumor JAK2/STAT3 signaalroute *. In menselijke equivalenten zal deze dosering van het extract echter 500 mg/dag zijn, waarvoor ongeveer 200 g droge grondstoffen nodig zijn *, wat duidelijk hoger is dan de aanbevolen dosering. Tegelijkertijd kunnen lage doses van het extract juist een oestrogene en proliferatieve werking hebben op ER+-cellen (MCF-7) *.
• Chinese glidkruid (Scutellaria baicalensis).
De belangrijkste medicinale componenten van het bovengrondse deel van het kalotje worden beschouwd als scutellarin, wogonine, baicalein en baicalin. Om de scheiding van baicaline en baicaleïne te bereiken, wordt water of methanol gebruikt als oplosmiddel om de eerste te extraheren, en aceton of ethylacetaat als oplosmiddel voor de tweede.
Wogonine, oraal ingenomen gedurende 4 weken in een dosering van 10 mg/kg, zonder toxiciteit, verminderde de groei van ER+-tumoren (T47D) die bij muizen waren geïnoculeerd met maximaal 88%, en de groei van ER–-tumoren (MDA-MB-231) met maximaal 48% *. Bij osteosarcoom vermindert wogonine in vitro (bij 40-80 μM) de CSC-update door de vorming van mammosfeeren te remmen en minimaliseert het potentiële risico van CSC's effectief *.
Baicaleïne remt de proliferatie, migratie en invasie van MDA-MB-231-cellen op een tijd- en dosisafhankelijke manier. Bij muizen geënt met MDA-MB-231-borsttumoren verminderde baicaleïne (100 mg/kg oraal) effectief de snelheid van metastasen en de grootte van metastatische laesies *.
Baicalin is in staat de invasie en migratie van borstkankercellen in vitro te onderdrukken, zonder echter hun levensvatbaarheid te beïnvloeden *. Die muizen getransplanteerd met kankerachtige TNBC-cellen (MDA-MB-231) die intraperitoneale injecties van baicalin (100 mg/kg) ontvingen, verminderden het aantal tumorformaties met de helft vergeleken met controlemuizen. De grootte van de tumorknobbeltjes was ook kleiner en het gewicht van de tumor was 4 keer lager *. Scutellarine en baicaline kunnen echter oestrogene en proliferatieve effecten uitoefenen in ER+-cellen (MCF-7), terwijl wogonine en baicaleïne (bij 50 μM) de groei van deze cellen remmen *.
Het volledige waterige extract van glidkruid remt zowel de glycolyse als de oxidatieve fosforylatie in tumorcellen *. In één klinische studie ondervonden 3 van de 27 patiënten met gemetastaseerde borstkanker regressie van de primaire tumor *. In een ander vergelijkbaar klinisch onderzoek slikten patiënten dagelijks 350 ml gestandaardiseerd kalotje-extract. Van de 21 deelnemers hadden er 7 een stabiele ziekte, en nog eens 5 ondervonden een verschillende mate van regressie *.
• Moederkruid (Tanacetum parthenium).
Parthenolide remt in vitro de vorming van MCF-7-mammosferen, evenals de proliferatie en vorming van kolonies van MCF-7-populatiecellen. Deze effecten waren het gevolg van remming van de NF-κB-activiteit in MCF-7-cellen die zowel in 2D-culturen als in mammosferen werden gekweekt *. Parthenolide en daarop gebaseerde geneesmiddelen verhogen de oxidatieve stress in kankercellen, onderdrukken de mitochondriale ademhaling en verhogen de expressie van RIP-1, wat leidde tot de dood van kankercellen door necrose.
Ondanks de hoge in vitro werkzaamheid is het therapeutische gebruik van parthenolide moeilijk vanwege de slechte oplosbaarheid ervan. Om dit probleem op te lossen werd een in alcohol oplosbaar dimethylamino-analoog van parthenolide (DMAPT) gecreëerd. Toediening van DMAPT (50 mg/kg p.o.) aan naakte muizen die xenotransplantaten van MDA-MB-231-cellen droegen, resulteerde in significante remming van de tumorgroei, verhoogde overleving van het dier en een duidelijke remming van longmetastasen *.
• Broccoli (Brassica oleracea).
Vergeleken met andere planten bevat broccoli de hoogste concentratie indool-3-carbinol (I3C). I3C verbetert de binding van nucleostemine (een oppervlaktemarker voor stamcellen van borstkanker) aan een tumorsuppressorremmer die interageert met het p53-eiwit, waardoor p53 vrijkomt en de kankercel in de richting van apoptose wordt gestuurd *. Een concentratie van 200 μM I3C voorkomt, dankzij de metaboliet 1-benzyl-I3C, vrijwel volledig de vorming van tumormammosferen in vitro. Om deze concentratie te bereiken kregen muizen getransplanteerd met met stamcellen verrijkte borsttumoren (10AT-HER2) subcutane injecties van I3C in een dosering van 300 mg/kg. In humane equivalenten zou dit 25 mg/kg of ongeveer 2'000 mg/dag zijn, terwijl in klinische onderzoeken de dosering van I3C niet hoger was dan 1'200 mg/dag *, en het maximale effect van het verbeteren van het oestrogeenmetabolisme dankzij I3C werd waargenomen bij 400 mg/dag dagen *.
• Knoflook (Allium sativum).
Diallyldisulfide (DADS), een in olie oplosbaar organosulfide in knoflookwortel, verzwakt het protumoreffect van linolzuur en versterkt het antitumoreffect van eicosapentaeenzuur in ER–-cellen (MDA-MB-231). Bij muizen geïmplanteerd met ER+ borsttumoren (KPL-1) veroorzaakten intraperitoneale injecties van DADS (1-2 mg) driemaal per week gedurende 35 dagen groeivertraging en een vermindering van 43% in het gewicht van de primaire tumor vergeleken met onbehandelde dieren *.
• Amarant driekleur (Amaranthus tricolor).
Amarantbladeren onderdrukken in vitro effectief de pro-inflammatoire enzymen COX-1 en COX-2 en vertonen antiproliferatieve activiteit tegen tumorcellijnen van de dikke darm, de borst, de longen en de maag *. Amarantbladeren in een dosering equivalent aan 1'300 mg/dag bij mensen toonden in experimenten van twee weken met muizen geïnoculeerd met Ehrlich-carcinoom een antiproliferatief effect vergelijkbaar met 5-fluorouracil *.
De noodzaak om zich te concentreren op kankerstamcellen maakt de aanbevolen lijst nog kleiner * *. Van de hierboven geselecteerde planten die succesvol waren tegen kankercellen van de tumorreeks, waren alleen de volgende succesvol tegen CSC's in vitro: wilde yam, fenegriek (actief bestanddeel – diosgenine); zoethout (actief ingrediënt – glabridine); moederkruid (actief ingrediënt – parthenolide); broccoli (werkzame stof – indool-3-carbinol), salie (werkzame stof – tanshinone), glidkruid (werkzame stof – baicaleïne).
Maar hoe succesvol al deze planten ook blijken te zijn in contact met kankercellen in tweedimensionale reageerbuisstudies, klinische onderzoeken kunnen veel minder bescheiden resultaten opleveren, en met een geheel andere effectiviteitsbeoordeling.
Beperking van cellulaire energie. Een van de tekenen van een kankercel is in de meeste gevallen een wijziging in de stofwisseling.
Terwijl cellen een kwaadaardige transformatie ondergaan, verschijnen de volgende kenmerken die verband houden met hun interne energie:
- Het aantal en/of de activiteit van de mitochondriën neemt af. Dienovereenkomstig neemt de functie van oxidatieve fosforylering (OF) af.
- Aan de andere kant nemen glycolyse en fermentatie, een minder efficiënte manier om energie te produceren vergeleken met OF, toe, wat resulteert in een beperkte energieproductie en verminderde thermische energie.
- Het intracellulaire niveau van Na+-ionen ten opzichte van het extracellulaire niveau van K+-ionen neemt toe. Dit vermindert de efficiëntie van membraan K/Na-pompen, die de cellulaire communicatie en celmembraandynamiek beïnvloeden * *.
Het transmembraanpotentieel van dergelijke cellen kan aanzienlijk worden verzwakt, waardoor deze zich gaat delen *. Een afname van de elektrische veldsterkte van het celmembraan veroorzaakt op zijn beurt veranderingen in de metabolische functies van de cel. Het negatief geladen veld rond de cel zal andere negatief geladen cellen afstoten, zoals rode bloedcellen en lymfocyten, en zal voorkomen dat het immuunsysteem kankercellen vernietigt *.
Op basis hiervan is het logisch om aan te nemen, en de resultaten van verschillende experimenten bevestigen dit, dat de beperking van de energieproductie normale cellen minder hard treft dan kankercellen, inclusief CSC's. Daarom kunnen veel strategieën die het energiemetabolisme verstoren, worden gebruikt als onderdeel van multi-target antikankertherapieën *.
Technieken voor het beperken van celenergie zijn al besproken in de sectie «Metabolische correctie» †. Hier herhalen we enkele punten:
Verminderde glucose-inname. De slimste suggestie is om het aantal calorieën te beperken, vooral eenvoudige suikers, die hoge bloedsuikerspiegels kunnen veroorzaken. Daarnaast kunt u de mogelijkheid overwegen om stoffen te gebruiken die de opname van koolhydraten belemmeren (metformine, silibinine, apigenine, quercetine), de productie van glucose in de lever verminderen (metformine), glucosetransporters naar cellen blokkeren (genisteïne, quercetine , kaempferol, diclofenac), onderdrukken de ophoping van glucose in cellen (essentiële oliën van citrusvruchten).
Onderdrukking van de glycolyse. Borstkankercellen worden gekenmerkt door een sterke afhankelijkheid van het glycolytisch metabolisme. Glycolyse maakt de productie van energie mogelijk in de hypoxische omgeving waarin tumorcellen zich bevinden. Dankzij glycolyse neemt de intracellulaire productie van bouwmateriaal voor de aanmaak van dochterkankercellen toe en wordt de noodzakelijke micro-omgeving gecreëerd voor hun invasie en metastase. Het glycolytisch metabolisme ondersteunt stamcellen van verschillende soorten kanker *. Remming van de glycolyse kan dus de effectiviteit van antitumortherapie aanzienlijk verhogen.
Glycolyseremmers verminderen de energiecapaciteit van kankercellen, evenals de intracellulaire productie van bouwmateriaal voor de creatie van een nieuwe cel.
Beperking van de mitochondriale ademhaling. Mitochondria zorgen niet alleen voor een economische productie van cellulaire energie. Ze spelen een cruciale rol in cellulaire processen zoals celsignalering, metabolisme, groeiregulatie en regulering van celdood. Dit zijn precies de processen die het tumorproces direct beïnvloeden. Inclusief de regulatie van stam- en kankercellen, hun identiteit, differentiatie en de keuze tussen leven en dood.
Hoewel borstkankercellen een hoge mate van anaerobe ademhaling hebben, behouden ze een aanzienlijke mate van aerobe ademhaling. Wanneer de aerobe ademhaling wordt onderdrukt, vertonen ze een verzwakt groeivermogen en een verhoogde gevoeligheid voor cytotoxische geneesmiddelen *. Daarom is het beheersen van mitochondriale functies een veelbelovende richting in de oncologie. Gezien het uitzonderlijke belang van de mitochondriën in het cellulaire leven kan de onderdrukking van hun functies echter niet langdurig zijn en is deze alleen geschikt tijdens een antitumortherapie.
Het proces van oxidatieve fosforylering kan worden verstoord door remmers van de elektronentransportketen, zoals menadion en salinomycine.
Het is belangrijk op te merken dat subpopulaties van kankercellen met de hoogste mitochondriale niveaus van oxidanten en mitochondriale biogenese het hoogste vermogen hebben om efficiënt mammosferen te vormen *. De mitochondriale biogenese en translatie kunnen echter worden geremd door bepaalde antibiotica zoals doxycycline, azitromycine, tigecycline en perviniumpamoaat *. Deze antibiotica remmen de eiwitsynthese door in te werken op de grote of kleine subeenheid van bacteriële ribosomen *, en pyriviniumpamoaat remt het proces van oxidatieve fosforylering *. Dankzij dit wordt het mogelijk om herhaaldelijk de levensvatbaarheid van tumor-initiërende cellen te verminderen.
Gecombineerde methoden. Omdat cellen van de ene energiebron naar de andere kunnen overschakelen om energie te produceren, is het remmen van alleen de glycolyse of het mitochondriale metabolisme waarschijnlijk minder effectief dan een combinatie van beide.
Zo creëren doxycycline en een hoge dosis vitamine C een dodelijke combinatie die zich richt op zowel het mitochondriale als het glycolytische metabolisme, wat uiteindelijk CSC's vernietigt *. Onderdrukking van de mitochondriale functie door doxycycline dwingt kankercellen om over te schakelen naar glycolytische ademhaling. Hierna laten een overdosis vitamine C, die de glycolyse blokkeert, hen op een hongerdieet achter. En oxidanten, die massaal worden gevormd als gevolg van de activiteit van vitamine C in de cel, werken er veel destructiever op in dan op normale cellen. Een alternatief voor vitamine C kan in dit geval berberine en parthenolide zijn *.
Nog effectiever is de toevoeging van azitromycine aan doxycycline en vitamine C. De combinatie van lage doses doxycycline en azitromycine vermindert het vermogen van CSC's om mammosferen te vormen met een factor 10 door ribosomen te remmen. Terwijl doxycycline het kleine mitochondriale ribosoom remt en azithromycine het grote mitochondriale ribosoom remt, vertonen ultrahoge doses vitamine C pro-oxidante effecten.
Het ascorbaatradicaal is doorgaans vrij stabiel, maar wordt in aanwezigheid van metaalionen zeer reactief. Vanwege het hoge ijzergehalte in kankercellen worden mitochondriën een gevoelig doelwit van het pro-oxidanteffect. Oxidatieve stress veroorzaakt door ascorbaat stimuleert de mitochondriale biogenese, waarvoor een verhoogd mitochondriaal metabolisme en ATP-productie vereist is. Als gevolg hiervan worden de mitochondriale functies van CSC's bijna volledig uitgeschakeld en is ATP aanzienlijk uitgeput, wat tot hun dood leidt *. Alle drie de componenten van deze combinatie hebben een beter veiligheidsprofiel dan de meeste standaard chemotherapiemiddelen, evenals vele jaren klinische ervaring en een zeer lage prijs.
Onderdrukking van invasie en metastase. Volgens moderne inzichten is metastase een proces waarbij kankercellen de zogenaamde epitheliale-mesenchymale transitie (EMT) ondergaan. EMT impliceert primitivisatie, dat wil zeggen een diepgaand verlies van celdifferentiatie. Als gevolg hiervan verwerven ze een hoge mobiliteit en komen ze in het bloed- en lymfesysteem terecht. Vervolgens verspreiden ze zich naar verre organen en weefsels van het lichaam, waar ze een omgekeerde transformatie ondergaan: mesenchymale-epitheliale overgang (MET), waardoor ze hun mobiliteit verliezen en vervolgens op een nieuwe plek beginnen te groeien.
• Metformine verzwakt de expressie van genen die betrokken zijn bij de hermodellering van de extracellulaire matrix van tumorweefsels, compliceert EMT en vermindert in het algemeen het algehele niveau van metastasen bij proefdieren *. Equivalente dosering: 3×500 mg.
• Piperine, een alkaloïde uit zwarte peper (Piper nigrum), verminderde de expressie van MMP-2/9 * en MMP-13 aanzienlijk en remde de migratie van 4T1-cellen in vitro *. Piperine remt in vitro de groei van TNBC-cellen en hormoonafhankelijke borstkankercellen, en versterkt ook de effecten van bestralingstherapie zonder de normale groei van borstepitheelcellen te beïnvloeden *. Injecties met piperine (5 mg/kg om de dag gedurende een maand) halveerden de groei van primaire borsttumoren bij muizen en remden ook significant de uitzaaiingen naar de longen *.
• Zoledroninezuur, een bisfosfonaat van de derde generatie, vermindert in vitro (bij 10 μM) niet alleen de proliferatie, maar ook de expressie van mesenchymale markers, en verhoogt ook de expressie van E-cadherine in TNBC-cellen *.
• Fisetin is een flavonol die vooral rijk is aan uien, tomaten, komkommers, appels, druiven, aardbeien, mango's en kaki *. Het interfereert met de belangrijkste regulatoren van EMT en zet dit om in MET, waardoor de metastase wordt geremd. Fisetin remt in vitro (bij 100 μM) de celproliferatie, migratie en invasie in TNBC-cellen (MDA-MB-231 en BT549), en subcutane injecties van fisetin in een dosering van 100 mg/kg gedurende een experiment van 3 weken halveerden de ontwikkeling van primaire TNBC-tumoren (MDA-MB-231) bij muizen *.
• Quercetine is een flavonol die veel voorkomt in granen, uien, appels en andere groenten en fruit. Intraperitoneale injecties van quercetine (50 mg/kg) verminderen de uitzaaiingen van melanoom naar de longen bij muizen *, en intraveneuze toediening van quercetine of zijn isovorm, pterostilbeen (20 mg/kg), vermindert de groei van levermetastasen bij muizen met 73% vergeleken met de controle *.
• Resveratrol is stilbeen, dat rijk is aan de schil van donkere druiven. Bij orale toediening (100 mg/kg gedurende 21 dagen) verminderde resveratrol significant de celadhesie, migratie, invasie en MMP-9-activiteit van geënte muizentumorcellen bij muizen. Ook het aantal longmetastasen daalde *. Orale toediening van resveratrol (50 mg/kg) gedurende 17 dagen remt de groei van het primaire tumorvolume met 60% vergeleken met de controle, en remt ook longmetastasen bij muizen met getransplanteerd melanoom *.
• Silymarine is flavonolignanen uit mariadistelzaden die in vitro antimetastatische effecten vertonen bij verschillende soorten kanker *. Silymarin heeft minstens 8 hoofdcomponenten, waaronder 7 flavonolignanen: silybin A, silybin B, isosilybin A, isosilybin B, silychristin, isosilychristin, silydianin en één flavonoïde – taxifoline. Omdat flavonolignanen slecht oplosbaar zijn in water, zijn hun conjugaten met fosfadylcholine (bijvoorbeeld Siliphos®) ontwikkeld. Een dagelijkse inname van drie weken (450 mg/kg) van een complex van silybine met fosfatidylcholine (silipid) vertraagde de ontwikkeling van spontane borsttumoren bij transgene muizen en verminderde het aantal borsttumoren *. Het complex verminderde significant het aantal muizen met longmetastasen, evenals de gemiddelde grootte van de metastasen, hoewel in een ander onderzoek de inname van silibinine via de voeding geen significant effect had op de tumorgroei *. Dosering silibinine: 1'400 mg/dag *.
• Salinomycine, een ionofoor antibioticum dat in de diergeneeskunde wordt gebruikt, verandert de expressie van genen die betrokken zijn bij metastasen, het vermogen tot tumorvorming en EMT-differentiatie * * *. Combinaties van salinomycine met traditionele chemotherapiemedicijnen (doxorubicine of paclitaxel), met anti-HER2-therapieën (trastuzumab of lapatinib), met resveratrol en met histondeacetylaseremmers onderdrukken synergetisch de groei van de primaire tumor * * * *. Salinomycine alleen doodt borst-CSC's in vitro 100 keer effectiever dan het standaard chemotherapiemedicijn paclitaxel *. Sommige gemodificeerde salinomycine-analogen waren zelfs effectiever dan salinomycine bij het remmen van TNBC-celmigratie (MDA-MB-231) *. Veel migratiegerelateerde parameters waren significant lager in MDA-MB-231-cellen na behandeling met salinomycine dan in controlecellen *.
• Diallyltrisulfide (DATS) remt in vitro (bij 10 μM) de migratie en invasie van TNBC-cellen (MDA-MB-231 en HS578t) door MMP2/9-metalloproteïnasen en de NF-κB- en ERK/MAPK-signaalroutes te remmen *. Dagelijkse dosis: 10 mg DATS, overeenkomend met 2 kruidnagels, d.w.z. 10 g rauwe knoflook *. Het gebruik van droge knoflook (3-4 eetlepels per dag) kan uw DATS-inname aanzienlijk verhogen zonder een knoflookgeur af te geven.
• Ellaginezuur, luteoline in granaatappelsap niet alleen de tumorgroei in vitro, maar verminderen ook de migratie van zowel oestrogeen-positieve (MCF-7) als oestrogeen-negatieve (MDA-MB-231) kankercellen tumoren zonder het gedrag van normale cellen te beïnvloeden *.
• Curcumine is een curcuminoïde uit kurkumawortel. Curcumine remt in vitro (bij 15 μM) migratie door de effectiviteit van E-cadherine te herstellen, een tumoronderdrukker die sterk wordt gereguleerd in borstkankercellen *, en vermindert de expressie van metalloproteïnasen MMP-2/9 *.
• Lycorine is een natuurlijke alkaloïde die voorkomt in de bloemen en bollen van Amaryllidaceae-soorten zoals narcissen (Narcisseae), sneeuwklokjes (Galantheae) en lycories (Lycoreae) *. Het is een krachtige inductor van apoptose en kan zowel mitochondriale als doodreceptor-gemedieerde apoptose in kankercellen induceren. Licorine heeft een matig kankerbestrijdend effect tegen verschillende kwaadaardige tumoren *, waaronder borstkanker, met een lage toxiciteit *. Intraperitoneale toediening van lycorine vertraagde de groei van borstkliertumoren bij experimentele muizen aanzienlijk.
• Anticoagulantia, zoals aspirine, verminderen de kans op trombose, en proteolytische enzymen, zoals bromelaïne, ontmaskeren veilig het bloedplaatjesmembraan van migrerende kankercellen.
• Antihistaminica hebben een dubbelzinnige werking. Een groot retrospectief onderzoek toonde aan dat langdurig gebruik van H1-antihistaminica zoals ebastine, loratadine of desloratadine de overleving significant verhoogde bij patiënten met zowel ER+ als ER– borstkankersubtypes, terwijl cetirizine en clemastine in de tegenovergestelde richting werken *.
Onderdrukking van angiogenese. Angiogenese wordt gereguleerd door het evenwicht tussen pro- en anti-angiogene factoren, die worden gecontroleerd in de extracellulaire ruimte.
Een belangrijke angiogene factor, vasculaire endotheliale groeifactor (VEGF), wordt gereguleerd door oestrogeen in zowel normaal * * als kankerachtig borstweefsel * *. Een andere krachtige angiogene factor is angiogenine, dat de proliferatie van endotheelcellen induceert na de nucleaire translocatie * *. Nucleaire translocatie van angiogenine is ook vereist voor de angiogene respons van VEGF en andere angiogene regulatoren *.
Angiogenine wordt ook gereguleerd door oestrogeen, net als VEGF * * *. Aan de andere kant worden ze tegengewerkt door endostatine, een van de belangrijkste anti-angiogene regulatoren. Endostatine remt de proliferatie en migratie van endotheelcellen en induceert apoptose van prolifererende endotheelcellen * * *. Endostatine kan ook de VEGF/VEGFR-signaleringsroute reguleren via directe effecten op tumorcellen of door andere anti-angiogene genen opwaarts te reguleren *. Estradiol vermindert en tamoxifen verhoogt de productie van endostatine * * *.
Sommige natuurlijke remedies kunnen worden gebruikt om angiogenese te onderdrukken.
• De combinatie van lijnzaad en tamoxifen is geëvalueerd in klinische onderzoeken * *. Hoewel de werkzame stof en het mechanisme ervan niet konden worden geïdentificeerd, werd vastgesteld dat gemalen lijnzaad (25 g/dag) de niveaus van VEGF of angiogenine niet verlaagde, maar, net als tamoxifen, de concentratie van endostatine in het borstweefsel aanzienlijk verhoogde.
• Genisteïne verbetert de adhesie van borstkankercellen, waardoor de celmigratie * wordt verminderd, en bij een dosering van 15 mg/kg de angiogenese * bij muizen wordt verminderd. De toevoeging van 750 mg genisteïne aan 1 kg voedsel vermindert het aantal uitzaaiingen bij muizen na chirurgische verwijdering van een borsttumor met een factor 10 *.
• Curcumine vermindert in vitro de activiteit van proteïnasen MMP-9 * en MMP-2 *, remt groeifactorreceptoren zoals EGFR en VEGFR. Curcumine, intraperitoneaal toegediend (300 mg/kg) aan muizen die waren geënt met triple-negatieve borstkankercellen (MDA-MB-231), vertoonde een significante afname van de expressieniveaus van proangiogene factoren en een afname van de microvasculaire dichtheid bij proefdieren gedurende 21 dagen *. Intraperitoneale injecties van curcumine (60 mg/kg) bij muizen met glioblastoom (U-87), geïmplanteerd in de schedel, verminderden het tumorvolume met 32% vergeleken met controles *. Tegelijkertijd daalde de enzymactiviteit van MMP-9 met 25%. Curcumine, gegeven in een dosis van 2% van de voedselinname gedurende 6 weken, induceert een duidelijke vermindering van de celproliferatie door apoptose, evenals een significante vermindering van de microvasculaire dichtheid bij AR+ prostaattumor (LNCaP) muizen *.
• EGCG (epigallocatechinegallaat) en andere polyfenolen uit groene thee reguleren de activiteit van een aantal belangrijke enzymen, wat leidt tot het blokkeren van de proliferatie van endotheelcellen en het onderdrukken van metastasen. Polyfenolen uit groene thee verminderen de angiogenese, vooral door de vasculaire endotheliale groeifactor en receptorfosforylering te verminderen *.
• Ellagotannines. Granaatappelextract, verrijkt met tot 37% ellagitanninen en 3,5% ellaginezuur, kan bij orale toediening (0,8 mg/dag) de tumor-geassocieerde angiogenese bij prostaattumorgeënte muizen (LAPC4) bijna verdubbelen *.
In menselijke equivalenten is dit 380 ml granaatappelsap per dag.
Intraperitoneale injecties van ellaginezuur (100 mg/kg gedurende 25 dagen) verminderden de groeisnelheid van getransplanteerde TNBC-borsttumor (MDA-MB-231) bij muizen met 6 maal *.
Het dagelijks consumeren van 1 glas granaatappelsap kan de verdubbelingstijd van prostaattumoren bij mannen verlengen van 15 tot 54 maanden *.
Interessant is dat het remmende effect duidelijk zichtbaar is in hypoxisch maar niet in normoxisch weefsel. Merk op dat ellagitanninen zelf niet in het lichaam worden opgenomen, maar in de vorm van ellaginezuur in de bloedbaan terechtkomen, waarin ze worden gehydrolyseerd onder invloed van darmmicroflora. Het combineren van ellaginezuur met fosfatidylcholine in een verhouding van 1:4 kan de biologische beschikbaarheid ervan verdubbelen *.
• Druivenpitproanthocyanidinen (20 μg/ml) vertragen in vitro de invasie van plaveiselcelcarcinoom van hoofd en nek door de EGFR-expressie te verminderen en de epitheliale-mesenchymale transitie om te keren *. Bij met prostaattumor geënte muizen (DU145) die gedurende 7 weken oraal werden behandeld met 100-200 mg/kg druivenpitextract (Traconol™) daalde de tumorproliferatie met tweederde en nam de apoptose 3-4 maal toe. Het aantal CD31-positieve cellen, die een marker zijn voor angiogenese, daalde met dezelfde hoeveelheid *. Druivenpitextract met ten minste 85% procyanidines en oraal toegediend aan muizen (equiv. aan 650 mg/dag) gedurende 3 weken vóór de implantatie van een borstkliertumor (MD-MBA-231) verminderde de snelheid van de daaropvolgende groei met 3 keer *.
• Eicosapentaeenzuur (EPA) en docosahexaeenzuur (DHA). Het verminderen van de verhouding tussen omega-6 en omega-3-vetzuren vertoont een significante specifieke anti-angiogene activiteit.
Ook de verhouding koper-zink is belangrijk. De meeste kankerpatiënten hebben een tekort aan zink en een teveel aan koper, en een teveel aan koper stimuleert de angiogenese in de tumor.
• Sommige planten worden traditioneel gebruikt als anti-angiogene stof: Zomeralsem (Artemisia annua), kruid; Maretak (Viscum album), bladeren en vruchten; Kurkuma (Curcuma longa), wortel; Glidkruid (Scutellaria baicalensis), wortel; Thee (Camellia sinensis), ongefermenteerde bladeren; Ginkgo (Ginkgo biloba), bladeren; Gember (Zingiber officinale), wortel; Ginseng (Panax), wortel; druivenpitextract (resveratrol en proanthocyanidine) * *.
Specifieke antiangiogene therapie, die aanvankelijk als een veelbelovende richting werd beschouwd, wordt nu ernstig in twijfel getrokken. Klinische observaties van de afgelopen jaren laten zien dat antiangiogene therapie alleen effectief kan zijn in combinatie met chemotherapie, maar niet alleen. Het proces van angiogenese zelf is geen onafhankelijk fenomeen; het is een regulerende reactie op een gebrek aan cellulaire voeding. Op basis van muismodellen concludeerden de onderzoekers dat een gebrek aan bloedtoevoer naar een tumor deze invasiever en meer metastatisch maakt, terwijl een tumor met voldoende bloedtoevoer rustiger is. Het algehele effect van monotherapie met krachtige anti-angiogene geneesmiddelen zoals bevacizumab kan dus het tegenovergestelde zijn van wat wordt verwacht * *.
De hierboven genoemde natuurlijke stoffen lijken echter een indirect anti-angiogene werking te vertonen; het wordt in verband gebracht met hun andere antitumoreffecten. Verminderde tumoractiviteit vereist minder voedingsstoffen, wat betekent dat de tumor minder bloedvaten hoeft te ontwikkelen.
Onderdrukking van stamkenmerken van kankercellen. Er bestaat een sterke veronderstelling dat het terugkeren van borstkanker wordt veroorzaakt door een kleine subpopulatie van tumorcellen, goed voor 0,1-2% van het totale aantal tumorcellen. Deze tumor-initiërende cellen hebben de eigenschappen van kankerstamcellen (Cancer Stem Cell, CSC) vanwege hun uitzonderlijke vermogen om de tumor zelf te vernieuwen en in stand te houden * * *, en een grote verscheidenheid aan stammen van kankercellen te produceren die zich in de tumor bevinden *.
De verzadiging van een tumor met kankerstamcellen houdt verband met de fenotypische kenmerken ervan. Bij de berekening van één CSC per 1'000 tumorcellen is dit: 1,1 voor luminaal subtype A (ER+/PR+, HЕR2–); 1,3 voor luminaal subtype B (ER+/PR+, HЕR2+); 8,6 voor HER2+-subtype (ER–/PR–, HЕR2+); en hoger dan 17,7 bij triple-negatieve borstkanker *. Opvallend is dat hoe hoger de concentratie CSC's in de tumor, hoe agressiever deze is en hoe slechter de prognose voor de ontwikkeling van de ziekte.
Hoewel traditionele chemotherapiemedicijnen het grootste deel van de tumorcellen vernietigen, veroorzaken ze processen die de versterking van CSC's bevorderen * *. De tumorigene cellen die de therapie overleven, bekend als de zijpopulatie (Side Population, SP), passen zich aan nieuwe omstandigheden aan, veranderen hun fenotype, ontwikkelen het vermogen om chemotherapiemedicijnen effectief uit de cel te pompen en zich te delen, waardoor een tumor ontstaat die resistent is tegen herhaalde chemotherapie *. Als het de kankerstamcellen * zijn die de behandeling overleven en de oorzaak zijn van het terugkeren van de tumor *, dan hangt het succes van de behandeling niet alleen af van het wegwerken van de primaire kankermassa of metastasen, maar ook van het richten van de behandeling op de CSC *.
Op basis van de specifieke eigenschappen van CSC's *
zijn er verschillende therapeutische doelen voorgesteld * * * * *:
- celoppervlakmarkers (CD44+/CD24–, integrinen) en functionele markers van CSC's (aldehydedehydrogenase * *);
- routes van zelfvernieuwing en differentiatie (Wnt/β-catenine, Hedgehog, Notch *);
- cytokinen en ontstekingsroutes (bijvoorbeeld IL-6, IL-8, TNF-α/NF-κB);
- TGF-β en epitheliale-mesenchymale transitieroutes (Twist en Snail);
- moleculen betrokken bij metastasen; voornamelijk CXCR4 of zijn ligand CXCL12;
- groeifactoren, hun receptoren en co-receptoren (zoals neuropiline-1) en signaalcomponenten (bijvoorbeeld tyrosinekinasen);
- geneesmiddelresistentie veroorzaakt door MDR/ABC-transporters (zoals ABCG2) en ALDH1.
CSC's vertonen opmerkelijke flexibiliteit en overlevingsvermogen bij een breed scala aan levensuitdagingen. Hierdoor is het onwaarschijnlijk dat monotherapie succesvol zal zijn, en om deze reden is een multimodale aanpak vereist voor betrouwbaar klinisch succes.
Via screening of andere observaties zijn verschillende geneesmiddelen geïdentificeerd die al in de menselijke en diergeneeskunde worden gebruikt en zich kunnen richten op CSC's; dit zijn salinomycine, etoposide, abamectine, nigericine, tesmilifene en andere *. Hiertoe behoren enkele klassieke geneesmiddelen zoals metformine * * *, tranilast * en thioridazine *, die al tientallen jaren worden gebruikt voor de behandeling van respectievelijk metabolische, allergische en psychiatrische ziekten.
Veel natuurlijke stoffen kunnen, hoewel zwak, ook interfereren met signaalroutes die cruciaal zijn voor het onderhoud van CSC's of voor het beheersen van het CSC-fenotype. Dit zijn in de eerste plaats curcumine, piperine, quercetine, pterostilbeen, resveratrol, berberine, catechines uit groene thee, sulforafaan, indool-3-carbinol, genisteïne, gingerol, vitamine E, vitamine D, retinoïnezuur, parthenolide, triptolide, shogaol, pterostilbeen, isoliquiritigenine, cyclopamine, celostrol, glabridine, coenimbin en vele andere *.
Van sommige Chinese medicijnen en hun actieve componenten is ook aangetoond dat ze giftig zijn tegen CSC's; dit is berberine uit de wortelstokken van Chinees gouddraad (Coptis chinensis); oxymatrine uit wortel van Sophora (Sophora flavescens); baicaleïne uit de wortel van Glidkruid (Scutellaria baicalensis); bufaline uit parotisgif en huidklieren van padden; CAPE van propolis en anderen *. Het gebruik van geschikte natuurlijke extracten zou dus tot op zekere hoogte de stamkarakteristieken van cellen in het bijzonder, en de ontwikkeling van tumoren in het algemeen, kunnen beïnvloeden.
Wnt/β-catenine zijn signaaleiwitten die betrokken zijn bij het coördineren van celgedrag in het lichaam. Ze moduleren de embryonale groei en reguleren celmigratie, proliferatie, differentiatie en overleving *. Abnormale stabilisatie van β-catenine wordt waargenomen bij meer dan 50% van de borstkankers *. Wnt/β-catenine-signalering bevordert genomische instabiliteit en weerstand tegen DNA-schade, en verleent CSC-resistentie tegen bestraling * * en chemotherapie * *. Reductie van β-catenine remt op significante wijze het tumorverwekkende vermogen van TNBC-cellen, zowel in vitro als in vivo, en vermindert ook de stameigenschappen van kankercellen *. Remmers van Wnt/β-catenine-signalering voorkomen dus de vorming van kolonies en mammosferen van borstkankercellen *.
• Salinomycine is een diergeneeskundig antibioticum dat de signaalroute Wnt/β-catenine *, Hedgehog en Notch remt *. Behandeling met salinomycine resulteert in verlies van expressie van CSC-geassocieerde genen geassocieerd met een slechte overlevingsprognose van de tumor *. Salinomycine is zeer effectief bij het uitroeien van CSC's, zowel in vitro als in vivo * *. Bij muizen geïnoculeerd met een TNBC-borsttumor (SUM159) vertraagde toediening van salinomycine (5 mg/kg intraperitoneaal gedurende 5 weken) de vorming van voelbare tumoren met 2 weken vergeleken met controledieren.
• Niclosamide* is een anthelminticum dat de Wnt-signaalroute remt zonder toxiciteit voor niet-tumorcellen te vertonen *. Dierproeven hebben aangetoond dat het met succes de activiteit van stamachtige borstkankercellen onderdrukt en de vorming van mammosferen van borstkankercellen voorkomt * *. Niclosamide remt niet alleen de Wnt/β-catenine-, mTORC1-, STAT3-, NF-κB- en Notch-signaalroutes, maar richt zich ook op de mitochondriën in kankercellen, waardoor celcyclusstilstand, groeiremming, autofagie en apoptose worden veroorzaakt *.
De orale dosering van niclosamide die in langdurige dierstudies wordt gebruikt, is het humane equivalent van 4-30 g/dag *. Helaas kunnen de slechte wateroplosbaarheid van niclosamide en de lage orale biologische beschikbaarheid resulteren in een te groot bereik aan serumconcentraties. Hoewel intraperitoneale toediening van 20 mg/kg niclosamide de groei van muizenborsttumoren (4T1) bij muizen onderdrukte zonder detecteerbare toxiciteit *, zijn de effecten van de injectie ervan bij mensen nog niet onderzocht.
• Acetaminophen, ook bekend als paracetamol, is een populair ontstekingsremmend, koortswerend en analgetisch medicijn dat zowel in vitro als in vivo de differentiatie van borstkankercellen induceert door remming van de Wnt/β-catenine-signaleringsroute. Subcutane toediening van paracetamol gedurende 28 dagen verminderde de groei van TNBC-geënte tumorcellen (MDA-MB-231) bij muizen aanzienlijk *. De dosering bedroeg hier 600 mg/kg, wat in humane equivalenten overeenkomt met 4'000 mg/dag, d.w.z. maximaal toelaatbare dagelijkse dosis voor volwassenen.
• Sulforafaan (50 mg/kg intraperitoneaal gedurende 2 weken) onderdrukte de activering van de Wnt/β-catenine-route, verminderde het aantal en de grootte van mammosferen, en halveerde de groei van menselijke ALDH+-borsttumoren die bij muizen waren geïnoculeerd *.
• Ivermectine, een bekend antiparasitair geneesmiddel, is bij lage doses een krachtige Wnt-routeblokker *. Ivermectine heeft ook een wisselwerking met verschillende andere doelwitten, waaronder multidrugresistentie-eiwit (MDR), Akt/mTOR-routes en enkele epigenetische deregulatoren, die zich voornamelijk richten op CSC's. Bovendien overwon ivermectine, in een zeer lage dosis die geen duidelijke cytotoxiciteit veroorzaakte, de geneesmiddelresistentie van kankercellen tegen chemotherapie door de expressie van P-glycoproteïne te verminderen *. De hoogste door de FDA goedgekeurde dosis is 200 μg/kg, maar ivermectine wordt goed verdragen door patiënten bij doses die 10 keer hoger zijn zonder merkbare toxiciteit *.
Net als salinomycine remt ivermectine de levensvatbaarheid van CSC-verrijkte celpopulaties (CD44+/CD24-- en cellen die in sferoïden groeien) sterker dan de algemene celpopulatie *, maar is veel minder giftig dan salinomycine. Het is zeer waardevol dat de antitumoractiviteit van ivermectine in vitro en in vivo wordt bereikt bij concentraties die klinisch haalbaar kunnen zijn op basis van farmacokinetische onderzoeken bij mensen *. Maar helaas zijn er geen rapporten gevonden over klinische onderzoeken met ivermectine tegen kanker.
• Curcumine en piperine – zowel afzonderlijk als in combinatie, remmen, door de Wnt-signalering te remmen, in vitro de zelfvernieuwing van borstkankerstamcellen en de vorming van de mammosfeer. In normale gedifferentieerde cellen veroorzaken ze geen toxiciteit *. Het combineren van beide stoffen versterkt de werking van elkaar. Wnt-signalering werd geremd door zowel curcumine als piperine – de helft bij 5 μM en volledig bij 10 μM.
• Vitamine D3 en zijn analogen remmen de Wnt-signalering in kankercellen in vitro door verschillende mechanismen *. Ze verminderen het aantal CSC’s in borsttumoren * en bevorderen ook de differentiatie van coloncarcinoomcellen door de β-cateninesignalering te remmen *. Orale toediening van een synthetisch analoog van vitamine D3 (0,1 μg/kg gedurende 36 dagen) halveerde de groei van het volume en het gewicht van getransplanteerde basaloïde borsttumoren bij muizen *.
• Resveratrol en pterostilbeen verminderen de vorming en levensvatbaarheid van de mammosfeer aanzienlijk, met als gevolg het op gang brengen van apoptose in kankerstamcellen. Resveratrol (100 mg/kg intraveneus), door de Wnt/β-catenine-route te onderdrukken, verminderde de groei van getransplanteerde borsttumoren (MCF-7 en SUM159) bij muizen met een derde, en verminderde de CSC-populatie onder tumorcellen. De stameigenschappen van kankercellen namen zo sterk af dat ze na herhaalde inenting van deze behandelde tumorcellen in secundaire muizen binnen 30 dagen slechts 1 tumor op 6 inentingen veroorzaakten, versus 6 tumoren in de controlegroep *. Muizen die werden behandeld met orale resveratrol (22,4 mg/kg om de dag gedurende 4 weken) vertoonden een significante vermindering van de groei van de getransplanteerde TNBC-tumor (MDA-MB-231) *. In menselijke equivalenten zijn de doseringen van deze twee experimenten respectievelijk 625 mg injectie en 140 mg oraal.
• Baicaleïne remt in vitro (bij 50 μM) en in vivo zowel Wnt/β-catenine als een speciaal AT-rijk bindend eiwit (SATB1) *. Bij met borsttumor geënte muizen (MDA-MB-231) verminderde orale toediening van baicaleïne (100 mg/kg gedurende 15 dagen) de levermetastasen significant.
• EGCG onderdrukt Wnt-signalering * en stamachtige celdeling bij inflammatoire borstkanker, hun invasieve fenotype en hun overleving *. Injecties van een oplossing die EGCG bevatte (16,5 mg/kg intraperitoneaal) vertraagden aanzienlijk de groei van getransplanteerde tumoren afgeleid van CSC's bij muizen. Quercetine versterkt in vivo de effecten van EGCG door de orale biologische beschikbaarheid van theepolyfenolen te verhogen en hun methylering te verminderen *.
• Diallyldisulfide (DADS), een in vet oplosbare component van knoflook, remt de groei en het metastatische potentieel van triple-negatieve borstkankercellen in vitro en in vivo door de β-catenine-signaleringsroute te inactiveren * *. Dosering: 2-10 g rauwe knoflook *.
• Genisteïne verzwakt in vitro de door β-catenine gemedieerde expressie van Wnt-doelgenen in borstepitheelcellen en bevordert celdifferentiatie *. Een voedingssupplement van genisteïne (250 mg per 1 kg voedsel) vertraagde de ontwikkeling van borsttumoren bij muizen *. Uit een meta-analyse van verschillende onderzoeken bleek dat de consumptie van sojaproducten na de diagnose van borstkanker de sterfte met 15% en het recidief met 21% verminderde, en dat deze percentages weinig afhankelijk waren van de menopauzestatus en de ER-status van de tumor *.
Notch is een membraanreceptor die een belangrijke rol speelt bij intercellulaire communicatie en celgedrag, en beslissingen over het lot van de cel, proliferatie, differentiatie en apoptose reguleert * *. Deze signaalroute reguleert de zelfvernieuwing en differentiatie van borststamcellen * *, en abnormaal hoge expressie van Notch-route-elementen * * bevordert de ontwikkeling van tumoren, waaronder borsttumoren. TNBC-tumoren (MDA-MB-231) hebben een significant hogere Notch-activiteit dan ERα+-tumoren (MCF-7 en T47D) of HER2+-tumoren (SK-BR-3) *.
Verschillende Notch-isovormen kunnen echter verschillende rollen spelen * en de ontwikkeling van tumoren bevorderen of onderdrukken. Notch1 lijkt bijvoorbeeld een oncogene rol te spelen bij borstkanker *, terwijl het uitschakelen van Notch2 de groei van TNBC-tumoren aanzienlijk versnelt *. De Notch4-isovorm lijkt het belangrijkst te zijn voor de vorming van mammosfeer *. Remming van de Notch4-signalering verminderde de CSC’s in de borsten en remde de tumorinitiatie volledig *. De Notch4-activiteit in borst-CSC's was, vergeleken met meer gedifferentieerde voorlopercellen, verhoogd, terwijl de Notch1-activiteit daalde. Dit kan erop wijzen dat selectieve remming van Notch1 en Notch4 effectiever kan zijn dan niet-selectieve remming van alle Notch-receptoren, inclusief met γ-secretaseremmers.
Sommige voedselcomponenten kunnen de Notch-signalering tot op zekere hoogte verzwakken.
• Retinoïnezuur vermindert de Notch-signalering via de doelgenen Hes2, Hey1, Hey2 en Hey5 * *. All-trans-retinoïnezuur (ATRA) is met succes gebruikt bij de klinische behandeling van acute promyelocytische leukemie door celdifferentiatie te bevorderen. Bij borstkanker onderdrukt ATRA in vitro Notch3 in TNBC-cellen (MDA-MB-231), maar heeft geen effect op Notch1 in HER2+-cellen (SK-BR-3) * *.
• Diallyltrisulfide (DATS) in vitro (bij 60 μM) onderdrukt door remming van de expressie van Notch-liganden Jagged-1 en Jagged-2 de levensvatbaarheid en vorming van kolonies van ER– (MDA-MB-231) en ER+ (MCF-7) cellen zonder normale cellen te beïnvloeden (MCF-12A) *. Tumorgeënte muizen (MCF-7) behandeld met DATS vertoonden een vermindering van het tumorvolume vergeleken met controledieren zonder duidelijke toxiciteit *. De therapeutische plasma-DATS-concentratie (30 μM) bij ratten werd bereikt na intraveneuze injectie van 10 mg DATS *.
• Curcumine in vitro (bij 30 μM) verhindert de vorming van sferoïden in slokdarmkankercellen door de activatie van Notch1, de expressie van zijn ligand Jagged-1 en zijn doelwitten Hes-1 te verminderen *. Muizen met een geënte pancreastumor (MIA PaCa-2), die oraal 250 mg/kg van een synthetisch analoog van curcumine (gedifloureerde curcumine) kregen, halveerden de grootte en het gewicht van de tumor vergeleken met de controlegroep als gevolg van een afname van de niveaus van eiwitten EZH2, CD44, EpCAM, Notch1 en Nanog *.
• Withaferine A, aanwezig in Ashwaganda (Withania somnifera), herstelt de verminderde Notch2-functie * en voorkomt door carcinogeen geïnduceerde borstkanker in muismodellen (equiv. 30 mg/dag) *, en remt het zelfvernieuwingsvermogen van CSC-borsttumoren in vitro (bij 1 μM) *.
• Genisteïne in vitro (bij 20 μM) onderdrukt de Notch1-activiteit in MDA-MB-231-cellen *. Suppletie van genisteïne aan ratten (250 mg/kg voedsel) vermindert de Notch2-expressie in borstepitheelcellen *.
• Oridonine, een diterpenoïde geïsoleerd uit bladeren van Isodon (Rabdosia rubescens) in vitro (bij 5 μM) remt de proliferatie van borstkankercellen van muizen (4T1) door de expressie van Notch1-Notch4-eiwitten te verminderen. Intraperitoneale injecties van oridonine (5 mg/kg gedurende 21 dagen) zonder merkbare toxiciteit veroorzaakten een vertraging in de groei van het tumorvolume (72%) en het tumorgewicht (84%) bij muizen *.
• Luteoline, een flavon gevonden in knolselderijwortel, vertoont in vitro (bij 100 μM) een hoog vermogen om Notch4-signalering te blokkeren en de proliferatie van TNBC te onderdrukken; vooral CSC-verrijkte populaties *.Apigenine en kaempferol laten vergelijkbare, maar iets slechtere resultaten zien. De toevoeging van luteoline aan paclitaxel verhoogt de cytotoxiciteit van laatstgenoemde bij TNBC. De aanbevolen dosering luteoline (LutiMax™) is 400-600 mg/dag zonder toxiciteit.
• Vitamine D en zijn synthetische analogen in vitro (10-100 nM) remmen de activiteit van Notch1-, Notch2-, Notch3-receptoren * * en andere componenten van de Notch-signaalas, waaronder NF-κB, Jag1, Jag2 en HES1 *.
• Resveratrol in vitro (bij 15 μM) vermindert de expressie van Notch1 en Notch2 in borst- en eierstokcellen * *, maar er is gemeld dat het hun expressie in glioblastoom- en meduloblastoom-cellen * * kan verhogen.
• Psoralidine, een coumarine dat voorkomt in zaden van Babchi (Psoralea corylifolia), remt Notch1-signalering in TNBC-cellen (MDA-MB-231) in vitro (bij 50 μM) *.
Hedgehog is een signaalglycoproteïne dat van cruciaal belang is voor de embryonale ontwikkeling, weefsel- en orgaanpatronen, stamcelvernieuwing, celproliferatie en -differentiatie, en weefselregeneratie en -herstel * *. Hedgehog-signalering vindt plaats via twee transmembraaneiwitten, Ptch1 en Smo. De Hedgehog-route komt sterk tot uiting in mammosferen *, wat wijst op de belangrijke rol ervan in CSC's.
• Itraconazol, een antischimmelmedicijn *, werd geïdentificeerd als een krachtige Hedgehog-remmer door het screenen van ongeveer 2'400 moleculen die eerder op toxiciteit waren getest of door de FDA waren goedgekeurd *. Bovendien kan itraconazol interageren met cyclopamine, dat wil zeggen dat beide geneesmiddelen blijkbaar op verschillende manieren op Smo inwerken. Een klinische fase II-studie toonde aan dat oraal itraconazol (2×200 mg gedurende 1 maand) bij patiënten met basaalcelcarcinoom van de huid de celproliferatie met 45%, de Hh-pathway-activiteit met 65% en het tumorgebied verminderde in vergelijking met de controlegroep. met 24% *. De combinatie van itraconazol en verapamil met 5-fluorouracil versterkte in vitro het therapeutische effect van laatstgenoemde aanzienlijk, voornamelijk als gevolg van een afname van de levensvatbaarheid en proliferatie van de cellen *. Opkomende resistentie tegen deze therapie kan worden overwonnen met PI3K-remmers *.
• Genisteïne is een sojabioflavonoïde. Genisteïne in vitro (bij 30 μM) vermindert ook de mammosfeer en vermindert het CSC-aantal MCF-7-kankercellen door neerwaartse regulatie van de Hedgehog-signaalroute. Met tumor geënte muizen (MCF-7) die werden behandeld met intraperitoneale injecties van genisteïne (50 mg/kg dagelijks gedurende 2 weken) hadden de helft van het tumorvolume en -gewicht *.
• Cyclopamine is een steroïde alkaloïde. Het richt zich op de Hedgehog-route, met name door de Smo-activering te remmen *, en remt de proliferatie van voornamelijk ongedifferentieerde cellen *. Bij borstkanker vermindert cyclopamine in vitro (bij 20 μM) de proliferatie van zowel ER+- (MCF-7) als ER–- (MDA-MB-231) borstkankercellen *. Bovendien vermindert cyclopamine de in vitro (bij 300 nM) mammosfeervorming en proliferatie van kankerstamcellen *.
Hippo is een signaalroute die de fysieke grootte van organen regelt door apoptose, celproliferatie en stamcelfunctie te controleren. De positieve rol van Hippo is het onderdrukken van de activiteit van twee transcriptionele co-activatoren: YAP en TAZ. Verschillende potentiële modulatoren van de Hippo-signaleringsroute worden hieronder vermeld, maar klinische onderzoeken met deze modulatoren bij borstkanker zijn niet gerapporteerd.
• Metformine is een biguanide dat wordt gebruikt voor type II-diabetes. Metformine fosforyleert YAP1 direct in vitro en in vivo *. Menselijke equivalente dosering – 1'500 mg * *.
• Scutellarin remde significant de groei van getransplanteerde ER+-tumoren (MCF-7), wat geassocieerd was met een afname van de YAP-expressie. Dagelijkse intraperitoneale injecties van scutellarine (5 mg/kg gedurende 3 weken) halveerden de gewichtstoename en het tumorvolume bij muizen, en de combinatie van scutellarine met 5-fluorouracil verlaagde deze waarde zelfs nog meer *.
• Apigenine in vitro (bij 30 μM) onderdrukt de migratie- en stamkarakteristieken van kankercellen door de YAP/TAZ-activiteit in TNBC-cellen (MDA-MB-231 en MDA-MB-436) te verminderen *. Inenting van muizen met met apigenine behandelde MDA-MB-231-cellen verminderde de kans op tumorvorming aanzienlijk, evenals de groei van het volume en gewicht ervan.
• Ivermectine is een antiparasitair middel dat de YAP1-activiteit remt in muismodellen (10 mg/kg intraperitoneaal gedurende 18 dagen), maar het werkingsmechanisme ervan is onbekend * *.
• Chlorpromazine, een ouder antipsychoticum, moduleert de Hippo-signalering en bevordert de proteasomale afbraak van YAP in vitro. Het is in staat om de stameigenschappen van borstkankercellen direct te remmen, waaronder de vorming van mammosfeer, de activiteit van aldehydedehydrogenase (ALDH1) en de bijbehorende genexpressie in bulktumorcellen en kankerstamcellen *.
• Simvastatine is een statine dat wordt gebruikt om het cholesterol te verlagen. Simvastatine in vitro (bij 1 μM) deactiveert YAP/TAZ door ze van de kern naar het cytosol te verplaatsen, waar ze worden vernietigd *.
• Dasatinib, een tyrosinekinaseremmer die voorkomt dat YAP complexeert *. Combinatie van dasatinib met statines in vitro (bij 1+1 μM) versterkt wederzijds de YAP/TAZ-remming in kankercellen *.
Nanog is een eiwit dat een centrale rol speelt bij het reguleren van het differentiatiepotentieel en de tumorigeniciteit van kankerstamcellen. De expressie van Nanog wordt gereguleerd door de signaalfactoren Oct4 en Sox2, en de overexpressie ervan bevordert de agressiviteit, invasie en metastase van tumoren.
• Metformine in vitro (bij 1-10 mM) verzwakt de door oestradiol geïnduceerde Oct4-expressie en vermindert dramatisch de grootte en het aantal mammosferen die zijn gegroeid in een 3D-model dat de ER+-borstkankerstamcelpopulatie (MCF-7) vertegenwoordigt *.
• Simvastatine en andere statines in vitro (bij 20 μM) onderdrukken de expressie van Oct4-genen *.
• Vitamine D in vitro (bij 100 nM) verlaagt de mRNA- en eiwitniveaus van Oct4 en onderdrukt de vorming van TNBC-mammosfeer (SUM159) *.
• Tretinoïne (ATRA) kan in vitro (bij 20 μM) de expressie van Oct4, Sox2, Nestin en CD44 onderdrukken, waardoor de proliferatie van CSC's wordt onderdrukt *.
AHR (aryl-koolwaterstofreceptor) is een transcriptiefactor die door veel kankerverwekkende factoren wordt geactiveerd.
• Omeprazol, een geneesmiddel dat wordt gebruikt bij maagzweren, vertoonde het beste in vitro effect * onder andere geteste AHR-agonisten, waaronder tranilast en sulindac. Hiervan verminderde alleen omeprazol de invasie van TNBC-kankercellen (MDA-MB-231) in vitro. Het remde ook significant de longmetastasen van TNBC in experimentele muizen in vivo (100 mg/kg) *.
• Tranilast is een niet-toxisch ontstekingsremmend en anti-allergisch middel, een AHR-antagonist. Tranilast remt in vitro (bij 200 μM) de proliferatie en vorming van kolonies en mammosferen van CSC’s die chemotherapie bij HER2+ en triple-negatieve borstkanker overleven *. Behandeling van met tumoren geïnoculeerde muizen (MDA-MB-231) met tranilast (300 mg/kg gedurende 21 dagen), vergeleken met controles, verminderde de groei van het tumorvolume met een factor drie en voorkwam metastasen in de longen. De equivalente dosis voor mensen zou 1'800 mg per dag zijn, wat zes keer de gewoonlijk voorgeschreven dosis is.
NF-κB is een transcriptiefactor die de expressie van immuunrespons-, apoptose- en celcyclusgenen regelt en is belangrijk voor verschillende centrale biologische processen, waaronder differentiatie tijdens embryogenese, ontstekings- en immunologische reacties, celproliferatie en overleving * * *. In het cytosol van de cel vormen NF-κB-eiwitten een complex met het IKB-eiwit en blijven in deze inactieve toestand totdat ze worden geactiveerd.
• Parthenolide remt in vitro (bij 5 μM) sterk de vorming van kankercelkolonies, evenals van mammosferen geïnoculeerd met borstkliertumoren (MCF-7) bij muizen door de NF-κB-activiteit te onderdrukken *. Bij muizen bij wie een ER–-tumor (MDA-MB-231) was geïmplanteerd, verhoogde een ethanoloplossing van parthenolide (40 mg/kg oraal), vergeleken met de controle, het overlevingspercentage na 45 dagen van 38% naar 73%, en combinatie parthenolide met docetaxel verhoogd is dit cijfer tot 90% *.
• Metformine in vitro (bij 300 μM) richt zich selectief op kankerstamcellen via fosforylatie van IκB *. De dosis voor mensen die overeenkomt met die bij muizen is 200 mg/dag.
• Genisteïne (bij 50 μM) en quercetine (bij 25 μM) hebben in vitro antiproliferatieve effecten in cellen die HER2 tot overexpressie brengen *.
• Diallyltrisulfide (DATS) remt ook in vitro NF-κB (bij 10-20 μM). Drievoudige negatieve kankercellijnen (MDA-MB-231 en HS578t) zijn er bijzonder gevoelig voor *. DATS zit in knoflook in een hoeveelheid van 1-3% van het totale gewicht. Zo kan een inname via de voeding van 10 g knoflook per dag (2 teentjes) zorgen voor voldoende DATS-concentraties in het lichaam (10 μM) *.
JAK/STAT zijn transcriptiefactoren die ervoor zorgen dat de cel reageert op signalen van groeifactoren. Blokkering van deze route resulteert in remming van zelfherstel en expressie van lipidenmetabolische genen *.
• Thymoquinone vermindert, in combinatie met paclitaxel, de JAK-STAT-signalering in vitro. Intraperitoneale injecties van thymoquinone (2,4 mg/kg per dag) en paclitaxel (1,25 mg/kg per week) onderdrukken krachtig de groei van muizen-TNBC bij muizen *.
• Metformine in vitro (bij 300 μM) remt STAT3-fosforylering in CSC's *.
• Vitamine Е (γ-tocotrienol) vermindert samen met simvastatine in vitro (bij 0,6+5 μM) het aandeel CSC's en de expressie van de signaalmediator STAT3 in borsttumoren *.
• Curcumine in combinatie met EGCG in vitro (bij 10+10 μM) remt specifiek de STAT3-fosfatering en de STAT3/NF-κB-interactie, waardoor het CSC-fenotype in de borstklier wordt onderdrukt *.
PI3K/Akt/mTOR is een signaalketen die een belangrijke rol speelt bij celoverleving, proliferatie, migratie, differentiatie en geneesmiddelresistentie * *. Bij tumoren wordt de activering van deze route vaak verstoord, waardoor kankercellen zich kunnen vermenigvuldigen en apoptose kunnen omzeilen.
• Knoflookextract in vivo interfereert met de PI3K/Akt-route en leidt tot een significante versterking van de cytotoxische effecten van chemotherapeutische middelen. Intraperitoneale injecties met knoflookextract verminderden de groei van borsttumoren met 30% bij behandelde muizen vergeleken met onbehandelde muizen *. De equivalente dosis voor de mens is 15 ml extract per dag verkregen uit ongeveer 4 teentjes knoflook.
• Quercetine in vitro (bij 60 μM) is een effectieve PI3K/Akt-remmer *. Intraperitoneale injecties van quercetine (15 mg/kg driemaal per week gedurende 13 weken) verminderden de groei van getransplanteerde TNBC-tumoren (MDA-MB-231) uit metastatische cellen bij muizen met 70% *. De equivalente dosis voor de mens is 120 mg/dag, wat driemaal de gemiddelde dagelijkse inname van quercetine via de voeding is.
• Sulforafaan in vitro (bij 40 μM) vermindert de clonogeniciteit van tumorcellen en heeft een sterk antiproliferatief effect via de PI3K/Akt-route *. Therapeutische niveaus van sulforafaan in serum kunnen worden bereikt door dagelijkse consumptie van 100 g rauwe broccoli.
• Metformine activeert in vitro (bij 300 μM) en in vivo (tot 2 g/dag) AMPK en remt het mTOR-enzym *.
• Metabolisch verteerbare voedingsmiddelen stimuleren mTOR. Dit geldt vooral voor zuivelproducten, dierlijke eiwitten, suiker, vruchtensappen, zoete dranken en andere voedingsmiddelen met een hoge glycemische lading. Een dieet dat dergelijke voedingsmiddelen uitsluit, zal dus zeker nuttig zijn.
MEK (mitogeen-geactiveerd proteïnekinasekinase). Hoewel mutaties in Ras/Raf/MEK/ERK-signaleringsroutegenen relatief zeldzaam zijn bij borstkankerpatiënten, komen hoge activiteit en hogere expressie van verschillende gensequenties in deze route vaker voor bij TNBC dan bij andere subtypes van borstkanker * * *. Meerdere adaptieve mutaties kunnen snel ongevoeligheid voor PI3K-routeremmers veroorzaken. Hiervoor is combinatietherapie nodig, bijvoorbeeld met MEK-remmers. Dubbele blokkade van PI3K- en MEK-signalering werkt synergetisch om de groei van basaloïde subtypes van borstkanker in vitro en in vivo krachtig te belemmeren *. Verschillende natuurlijke stoffen zijn ook in staat om de Ras/Raf/MEK signaalroute met enig succes in vitro te remmen *, maar zijn grotendeels niet beschikbaar. En de beschikbare hebben een zeer onbeduidend effect.
• Anthocyanen uit zwarte rijst in vitro (bij 200 μg/ml) onderdrukken de Ras/Raf/MEK-signaalroute en voorkomen metastase van HER2+-tumoren * *. Orale toediening van anthocyanidinen (150 mg/kg) vertraagde de groei en onderdrukte de longmetastasen van een TNBC-tumor (MDA-MB-453) geënt in muizen *.
• Tanshinone IIA, aangetroffen in saliewortel, vermindert de expressie van Ras, Raf, VEGFR, HER2, MEK en ERK in vitro*. Dosering: 80 mg/dag *. Combinatie met piperine kan de biologische beschikbaarheid van tanshinon verbeteren.
• D-limoneen, een triterpenoïde die voorkomt in citrusschillen, vermindert de expressie van Ras en Raf *.
In onderzoeken bij ratten resulteerde 2,5% perillylalcohol in de voeding in een regressie van 81% van de kleine en 75% van de gevorderde door carcinogeen geïnduceerde borstcarcinomen *.
Bij muizen met een getransplanteerde borsttumor leidden injecties van perillylalcohol (75 mg/kg intraperitoneaal om de dag gedurende 6 weken) tot zowel onderdrukking van de groei van de primaire tumor als onderdrukking van de verspreiding van metastasen naar de lymfeklieren *.
Uit klinische fase II-onderzoeken bleek echter dat de inname van aanvaardbare doses perillylalcohol bij patiënten met borstkanker geen voordeel oplevert *.
Dagelijkse dosering: van 3×1,6 tot 4×2 g *,
maar niet hoger. Toediening via de neus door inhalatie is comfortabeler en effectiever dan toediening via de mond (oraal), aangezien de inname van zulke grote hoeveelheden perillylalcohol maag-darmklachten, vermoeidheid en andere ongewenste bijwerkingen veroorzaakt.
Twist, Snail zijn twee transcriptiefactoren die betrokken zijn bij EMT en de metastase versterken.
• Fisetin onderdrukt de expressie van Snail1, Zeb1, Twist1 en Slug in melanoomcellen *. De combinatie van fisetin (20 μM) met sorafenib (5 μM) is zelfs nog effectiever in het verminderen van celmigratie en invasie in vitro. Experimenten met melanoommuizen (45 mg/kg fisetin en sorafenib oraal) bevestigden de resultaten van deze onderzoeken *.
• Iraanse mumijo veroorzaakt in vitro remming van EMT en onderdrukking van metastasen in borstkankercellen, voornamelijk als gevolg van onderdrukking van TGF-β1-activiteit, maar ook als gevolg van onderdrukking van de activiteit van Twist1, Notch1 *. Het kankerbestrijdende effect van mumiyo was meer uitgesproken tegen de MDA-MB-231-cellijn dan tegen MCF-7 en vertoonde geen enkel effect op normale borstcellen.
• Zoledroninezuur (bij 10 μM) vermindert in vitro de expressie van Twist en Snail in TNBC-borstkankercellen *.
• Entinostat kan in vitro de epitheliale-mesenchymale transitie (EMT) van TNBC-borstkankercellen (MDA-MB-231 en HS578t) afschaffen door de associatie van Twist and Snail met de E-cadherine-promoter te verminderen *.
ALDH1 (aldehyde dehydrogenase 1) is een karakteristieke functionele marker van CSC's bij borstkanker, die wordt gebruikt voor de identificatie ervan. Positieve ALDH1-expressie is verantwoordelijk voor ongeveer 17% van de luminale A-subtypen, 21% van de luminale B-subtypen, 54% van de HER2-subtypen, 33% van de basaloïde subtypen en 18% van de niet-basaloïde subtypen * *.
ALDH speelt een belangrijke rol bij de differentiatie van stamcellen via retinoïnezuur *. Het verhoogt de therapeutische weerstand van kankercellen omdat het chemotherapiemedicijnen zoals cyclofosfamide metabolisch kan inactiveren *.
Ten slotte zou NADH geproduceerd door ALDH een alternatieve energiebron kunnen zijn voor de productie van ATP in kankercellen * *. Remming van aldehyde dehydrogenase (ALDH) met gossypol in combinatie met remming van mitochondriaal complex I met fenformine resulteerde in een uitputting van de ATP-productie in kankercellen tot 80%, terwijl normale cellen geen verlies aan ATP-productie hadden *. Deze manipulatie ging gepaard met regressie van de groei van de getransplanteerde tumor bij dieren. Gossypol kan echter geen goede keuze voor mensen worden genoemd.
• Disulfiram, dat al vele jaren wordt gebruikt om alcoholisme te behandelen, is de krachtigste bekende ALDH1-remmer. De effectiviteit ervan is bewezen bij muizen met een dosering van 200 mg/kg, wat bij mensen gelijk is aan 15 mg/kg *. De dagelijkse dosering voor mensen zou daarom ongeveer 1 g/dag bedragen, wat tweemaal de aanbevolen dosering voor disulfiram is en aanleiding geeft tot bezorgdheid over de toxiciteit ervan, zelfs bij een orale absorptie van slechts 20%. In klinische onderzoeken werd een orale dosering van 120 mg/dag gebruikt, maar monotherapie met disulfiram was niet erg succesvol bij terminaal zieke patiënten *. Tegengiffen voor disulfiram zijn ascorbinezuur en H1-blokkers.
• Tretinoïne (ATRA) versterkt, door ALDH1 te remmen, het in vitro effect van bestraling en chemotherapie (doxorubicine/paclitaxel) op TNBC-cellen *. In experimenten met muizen met getransplanteerde eierstoktumoren verminderde tretionine (0,1 mg/kg 1 keer per 2 dagen gedurende 10 dagen) de tumorgroeisnelheid bij behandelde dieren met een factor 6 vergeleken met onbehandelde dieren *. In menselijk equivalent zal deze dosering 0,6 mg/dag zijn.
• Sulforafaan vermindert in vitro (bij 1-5 μM) het aandeel ALDH+-cellen met 65-80%, en vermindert de grootte (8-125 maal) en het aantal (45-75%) van de primaire mammosferen in borsttumoren. Bij muizen ingeënt met TNBC-tumoren (SUM159) verminderde sulforafaan (50 mg/kg intraperitoneaal gedurende 2 weken) het aantal ALDH+-cellen met meer dan de helft *. De equivalente injectiedosis bij mensen voor deze experimenten zou 4,2 mg/kg zijn, of 320 mg/dag voor een persoon van 75 kg.
• Acetylsalicylzuur (aspirine) kan in vitro de expressie van ALDH1, SOX2, OCT4 en NANOG in kankerstamcellen van muizen (4T1) verminderen. Als gevolg hiervan wordt het vermogen van borstkankercellen om mammosferen te vormen aanzienlijk verminderd *. In experimenten met muizen met een getransplanteerde tumor werd een dosering van 100 mg/kg gebruikt, wat in humane equivalenten 600 mg/dag zou zijn.
IGF-1 (insuline-achtige groeifactor 1) is een peptide dat, in zijn vrije (d.w.z. niet geassocieerd met glycoproteïnen) vorm, de celdeling stimuleert en apoptose onderdrukt * *. Meta-reviews van onderzoeken geven aan dat plasma-IGF-1-concentraties positief geassocieerd zijn met het risico op borstkanker; dit geldt in ieder geval voor oestrogeenpositieve tumoren. Vrouwen met de hoogste IGF-1-niveaus hadden een 28% hoger risico op het ontwikkelen van borstkanker dan vrouwen met de laagste niveaus, ongeacht hun menopauze *. Sommige onderzoeken suggereren dat IGF-1 voor borstkankercellen een krachtigere groeistimulator kan zijn dan estradiol *.
• Een veganistisch dieet kan de plasma-IGF-1-concentraties verlagen * *. Terwijl dierlijke eiwitten de IGF-1-niveaus verhogen, verlagen de meeste plantaardige eiwitten deze, hoewel dit laatste afhangt van het type en de hoeveelheid geconsumeerde eiwitten. Uit een aantal onderzoeken is gebleken dat de IGF-1-waarden stijgen als gevolg van een verhoogde inname van totaal eiwit *, suiker, melkeiwit en calcium *, rood vlees, totaal en verzadigd vet *. Omgekeerd worden plantaardige en eiwitarme diëten geassocieerd met lagere niveaus van totaal IGF-1. Uit retrospectief onderzoek blijkt dat de gemiddelde serum-IGF-1-concentraties bij veganistische vrouwen 13% lager zijn dan bij vleeseters en vegetariërs *.
• Eiwitarm dieet. Manipulatieve onderzoeken bevestigen het verband tussen eiwitinname en IGF-1-niveaus: het verminderen van de dagelijkse eiwitinname van gemiddeld 1,67 naar 0,95 g per 1 kg lichaamsgewicht binnen 3 weken leidde tot een afname van IGF-1 in het serum van gezonde mensen uit 194 ng/ml tot 152 ng/ml, d.w.z. met 28% *. Tegelijkertijd vermindert zelfs langdurige caloriebeperking de concentratie IGF-1 in het serum van gezonde mensen niet als de eiwitinname hoog blijft.
Een rijke voedingsbron van IGF-1 zijn melk en zuivelproducten, waarvan de consumptie de concentratie in het bloed kan verdubbelen *. Het dagelijks consumeren van een glas melk verhoogt het risico op borstkanker zeven keer meer dan het dagelijks consumeren van een portie gekookt vlees van 85 gram *.
• Een vetarm dieet gecombineerd met matige lichaamsbeweging verminderde IGF-1 in het serum van ouderen met 20% in slechts 11 dagen, en het volgen van deze kuur gedurende meerdere jaren kan dit met 55% verminderen *.
• Lichamelijke activiteit in combinatie met een vetarm (10-15% van de totale calorieën), vezelrijk (30-40 g per 1'000 kcal) dieet verlaagt de serumspiegels van oestrogeen (met 34-37%), insuline (met 29%) en IGF-1 (met 19%) bij postmenopauzale vrouwen *, waardoor het risico op borstkanker afneemt en de overlevingskansen verbeteren *.
Er moet echter aan worden herinnerd dat pogingen om kankerstamcellen te remmen tot op zekere hoogte de functie van normale stamcellen kunnen beïnvloeden.
Differentiatie stimuleren. Zoals de praktijk laat zien, mislukt een strategie die uitsluitend gericht is op het vernietigen van kankercellen vaak. Ondanks het aanvankelijke succes bij het verkleinen van tumoren, blijven kankerstamcellen zichzelf doorgaans vernieuwen. Een alternatieve strategie is het stimuleren van terminale celdifferentiatie, d.w.z. ze overbrengen naar een volwassen staat met verlies van het vermogen om ongecontroleerd te verdelen. Verhoogde differentiatie van onrijpe cellen maakt ze gevoeliger voor chemotherapie en minder actief bij metastasen.
Tot op heden zijn er zeer weinig moleculen bekend die differentiatieprocessen effectief kunnen verbeteren. En bijna allemaal zijn ze niet getest in een klinische omgeving.
• Vitamine А (ATRA als tretionine) is het krachtigste en meest bewezen middel voor het bevorderen van celdifferentiatie. Dosering en regime – volgens het recept van de arts (voor leukemie, gebruik 40 mg tweemaal daags gedurende 30-90 dagen). Hoewel ATRA (all-trans-retinoïnezuur) op grote schaal wordt gebruikt om verschillende soorten kanker te behandelen, kan het cytotoxiciteit en resistentie tegen geneesmiddelen veroorzaken als het in hoge doses wordt gebruikt bij borstkanker *.
Door ATRA te combineren met andere natuurlijke stoffen kunt u de therapeutische dosis ervan verlagen. Curcumine en ascorbinezuur verhogen dus de in vitro activiteit van retinoïnezuur en helpen de ontwikkeling van retinoïderesistentie in MCF-7-borstkankercellen te overwinnen * *. De combinatie van ATRA en omega-3-vetzuren werkt in vitro synergetisch om de groeionderdrukking van zowel oestrogeen-positieve als oestrogeen-negatieve tumoren te verbeteren *. Andere stoffen van natuurlijke oorsprong zijn veel zwakker. Helaas kunnen kankercellen zeer snel resistent worden tegen deze therapie.
• Vitamine D3 reguleert de cellulaire differentiatie * en zorgt voor een synergetisch effect met retinoïnezuur *. In in vitro-experimenten (bij 100 nM) onderdrukt het de Notch-signalering, waardoor differentiatie van drievoudige negatieve borstkankercellen wordt veroorzaakt *, en vermindert het ook het aantal kankerstamcellen in borsttumorweefsel *.
• Calcium verschaft de voorwaarden voor de uiteindelijke differentiatie van borstkliercellen; Wanneer het calciumniveau onder een kritiek punt daalt, differentiëren de cellen niet * *. Dit betekent niet dat u calcium in grote hoeveelheden moet innemen; dit betekent dat het adequate niveau in het lichaam moet worden gewaarborgd.
• Paracetamol is een ontstekingsremmend, koortswerend en analgetisch geneesmiddel. Uit een screening van 250 klinisch gebruikte geneesmiddelen bleek dat paracetamol in vitro de differentiatie van TNBC-cellen (MDA-MB-231) induceert door de Wnt/β-catenine-signaleringsroute te remmen en de expressie van de multimedicijnresistentie-membraanpomp MRP te onderdrukken. Subcutane injecties met paracetamol (600 mg/kg) remden de groei van de getransplanteerde MDA-MB-231-tumor bij dieren niet slechter dan doxorubicine (4 mg/kg), en hun combinatie werkte synergetisch, waardoor de groei van het tumorvolume vier keer werd vertraagd *. De dosis paracetamol die in dit onderzoek werd gebruikt (humaan equivalent 4 g/dag) ligt echter op de limiet van de gebruikelijke klinische dosis en kan hepatotoxiciteit veroorzaken *.
• Arseentrioxide (As2O3) kan in vitro bij lage concentraties (0,1-1 μM) de differentiatie van leukemiecellen (HL-60) aanzienlijk bevorderen, maar bij hogere concentraties (2,5-5 μM) gaat dit vermogen verloren *. Lage concentraties arseentrioxide in vitro (bij 0,5 μM) leiden tot een matige afname van de levensvatbaarheid en verhoogde differentiatie van verschillende borstkankercellijnen (MCF-7, MDA-MB-231, T-47D en BT20). Bij hogere concentraties begint het proapoptotische effect van arseentrioxide te verschijnen, waarbij de MCF-7- en MDA-MB-231-lijnen gevoeliger zijn dan de T-47D- en BT-20-lijnen.
Een concentratie van 2 μM arseentrioxide in borstkankercellen is het meest effectief en omvat drie therapeutische mechanismen: groeiremming, differentiatie en apoptose. De equivalente dosering voor mensen, die overeenkomt met de arseentrioxideconcentraties in deze experimenten, zou 0,15 mg/kg zijn *. Bovendien kan arseentrioxide de ERα-expressie in ERα-negatieve borstkankercellen herstellen en deze gevoelig maken voor endocriene therapie *.
• Butyraat, ook bekend als boterzuur, een van de vetzuren met een korte keten die door darmbacteriën worden geproduceerd, toonde in vitro een hoog vermogen om kankercellen te differentiëren. In klinische onderzoeken vertoonde de systemische toediening van butyraat aan patiënten met acute leukemie, zelfs in hoge doses (500 mg/kg), echter geen enkele effectiviteit vanwege de zeer snelle metabolisatie (ongeveer 6 minuten) *. Lokaal bestuur was effectiever bij darmkanker.
• Lijnzaad verbetert de differentiatie van de borstklieren bij muizen. Het voeren van muizen met een dieet bestaande uit 10% lijnzaad of een gelijkwaardig niveau van de belangrijkste lignan ervan stimuleerde de celdifferentiatie en de vorming van gezonde borstklieren bij de dieren aanzienlijk *.
• Mefloquine, een antimalariamedicijn, stimuleert in vitro (bij 10 μM) de stamceldifferentiatie *.
• Fytinezuur (IP6, inositolhexafosfaat) – een vitamine die voorkomt in groenten en granen, bevordert niet alleen de celproliferatie, maar bevordert ook in vitro (bij 10 mM) differentiatie van kwaadaardige cellen *. Dieren die IP6 dronken, vertoonden een significante vermindering van de incidentie en de veelheid van tumoren *.
• Lycopeen (bij 5 μM) *, quercetine (bij 5 μg/ml) en genisteïne (bij 15 μg/ml) * verhogen de in vitro expressie van Cx43 en onderdrukken de proliferatie van borstkankercellen.
Regulatie van metabolische routes. De ontwikkeling, progressie en metastase van borstkanker vindt meestal plaats door de activering van verschillende signaalroutes *, zoals de oestrogeenreceptor, groeifactorreceptor, cellulaire metabolische routes en interacties daartussen.
Borstkanker is het resultaat van reeds bestaande aangeboren of, vaker voorkomend, aangeboren-achtige stofwisselingsstoornissen *. De daaropvolgende herstructurering van het metabolisme van kankercellen is een reactie op de eisen van de zich ontwikkelende tumor – van de pre-tumor tot de gevorderde staat. Bovendien vertonen verschillende tumortypen en -subtypen een verschillend metabolisme *. Drievoudige negatieve borstkanker maakt dus voornamelijk gebruik van de productie van glycolytische energie, terwijl ER-positieve borstkanker gebruik maakt van de productie van mitochondriale energie. De meeste subtypen versterken echter in verschillende mate de glycolyse en glutaminolyse, die essentieel zijn voor celproliferatie en geschikte therapeutische doelen kunnen zijn.
Voor de creatie van een nieuwe cel zijn vetzuren nodig om de celwand te vormen, nucleotiden en aminozuren om de eiwitten van de cel te creëren, en energie om het constructieproces aan te drijven.
• Radicicol is een antibioticum dat in vitro (bij 13 μM) ATP-citraatlyase bindt en remt *. Een ander antibioticum, antimycine A, in vitro (bij 30 μM), vermindert naast het onderdrukken van ATP-citraatlyase ook de ATP-productie in de mitochondriën.
• Epigallocatechinegallaat (EGCG) * en rozemarijnzuur * remmen de pentosefosfaatroute van de glycolyse om de nucleotideproductie in vitro te remmen, en sugiol, aangetroffen in saliewortel, doet hetzelfde in vivo (equiv. van 200 mg/dag) *.
Bioversterkers. Biologische beschikbaarheidsversterkers zijn stoffen die op zichzelf geen significante farmacologische activiteit hebben, maar in combinatie met therapeutische stoffen hun biologische beschikbaarheid en effectiviteit vergroten.
Sommige plantaardige stoffen verbeteren de farmacokinetische parameters van veel farmaceutische geneesmiddelen *. Ze helpen de belangrijkste redenen voor de slechte effectiviteit van geneesmiddelen te overwinnen: slechte orale absorptie, snel first-pass metabolisme door de lever en efficiënt pompen van actieve stoffen uit cellen. Kruidenbioversterkers zijn gemakkelijk verkrijgbaar, veilig, verminderen de medicijndosering en minimaliseren de behandelingskosten.
• Piperine, de belangrijkste alkaloïde die voorkomt in de zaden van Zwarte peper (Piper nigrum) en Lange peper (Piper longum), is de meest bestudeerde bioversterker, die ook een onafhankelijk antitumoreffect heeft *. Piperine heeft een dubbele werking: het helpt niet alleen bij de opname van geneesmiddelen in de darmen, maar voorkomt ook dat P-glycoproteïne deze uit de cellen verwijdert *. Bovendien remt piperine de glucuronidering *. Piperine verbetert de bioactiviteit van verschillende categorieën geneesmiddelen: antibiotica, antivirale middelen, antischimmelmiddelen, ontstekingsremmende middelen, cardiovasculaire middelen en andere. In verschillende dierstudies versterkte piperine ook de effectiviteit van EGCG * en curcumine *. De humane equivalente dosis piperine in deze experimenten zou ongeveer 120 mg/dag zijn, maar het kan nodig zijn dat deze minstens 500 mg/dag * bedraagt.
• Curcumine, de belangrijkste curcuminoïde uit Kurkuma (Curcuma longa), kan worden gebruikt als bioversterker voor antimicrobiële geneesmiddelen en geneesmiddelen tegen kanker. Bovendien staat het zelf bekend om zijn antitumorale eigenschappen. Curcumine remt de levergeneesmiddelmetabolisme-enzymen (CYP3A4) * en schaadt P-glycoproteïne, dat medicijnen uit cellen verwijdert. Het versterken van het effect van de belangrijkste therapeutische middelen wordt niet onmiddellijk bereikt tijdens het gebruik ervan, maar pas na enkele dagen voorafgaand gebruik van curcumine *. Curcumine verhoogde de biologische beschikbaarheid van docetaxel met ongeveer een factor acht bij ratten *. De humane equivalente dosis zal ongeveer 1'200 mg/dag zijn * *.
• Quercetine is een flavonoïde die in de grootste hoeveelheden voorkomt in vlierbessen, veenbessen, uien, appels, citrusvruchten, groenten, bladeren en sommige granen. Quercetine remt tegelijkertijd cytochroom CYP3A4 en P-glycoproteïne *, waardoor het een tweeledig effect heeft op het verhogen van de biologische beschikbaarheid van geneesmiddelen. Hierdoor neemt de biologische beschikbaarheid van tamoxifen met 15% toe vergeleken met de controlegroep *. In andere onderzoeken versterkte quercetine de therapeutische effecten van doxorubicine *, irinotecan * en etoposide * bij dieren aanzienlijk. Menselijke equivalente doseringen in deze onderzoeken waren 150-200 mg/dag.
• 6-gingerol is een polyfenol dat voorkomt in de wortel van gember (Zingiber officinale), en dat een ontstekingsremmende * en antitumorale * werking heeft. Gemberextract versterkte het antitumoreffect van doxorubicine bij muizen met mammacarcinoom *. De dosering gemberextract als bioversterker voor mensen is 10-30 mg/kg, d.w.z. ongeveer 1'500 mg/dag *.
• Luteoline en andere polyfenolen uit zaad van Komijn (Cuminum cyminum) werken door het remmen van P-glycoproteïne *, maar vertonen ook zelf antitumoreffecten *. De effectieve dosis komijnextract is 10-30 mg/kg, en luteoline 2-20 mg/kg *.
• Carvon en limoneen zijn terpenoïden die voorkomen in zaad van Karwij (Carum Carvi). Karwijzaadextract vertoont zijn bioversterkereffect bij een dosering van 5-100 mg/kg, en het actieve deel – bij 1-55 mg/kg *.
• Glycyrrhizine is een saponineglycoside dat wordt gewonnen uit de wortels en kruipende scheuten van Zoethoutplant (Glycyrrhiza glabra). Glycyrrhizine bevordert de beweging van geneesmiddelen door celmembranen naar cellen en verhoogt hun concentraties in het plasma, waardoor het effect van antibiotica, anti-infectieuze middelen en antitumormiddelen (zoals Taxol™) effectief wordt versterkt. De versterkende activiteit van glycyrrhizine hangt af van de omzetting ervan door het bacteriële enzym β-glucuronidase in de darmen in glycyrrhetinezuur.
Helaas zijn er zeer weinig publicaties over dit onderwerp en zijn er vrijwel geen klinische onderzoeksresultaten die passende aanbevelingen kunnen doen. Het is onmogelijk om in elk specifiek geval de exacte dosering van de versterker te bepalen, omdat het varieert afhankelijk van vele factoren, waaronder het type geneesmiddel dat wordt gebruikt.
Naast chemische bioversterkers worden ook andere, nog onbewezen methoden voorgesteld om de lokale absorptie van therapeutische middelen te verbeteren:
- bestraling van het doelgebied met rood licht uitgezonden door de LED (~620 nm);
- krachtige massage van het doelgebied (minimaal 1-2 minuten 4 keer per dag);
- het aanbrengen van een negatieve elektrische pool op het doelgebied, en een positieve pool op het afgelegen gebied, indien toegestaan (18-45 volt, 4 keer per dag);
- het aanbrengen van de zuidpool van een magneet op het doelgebied van het lichaam (800-3'000 gauss, gedurende 1-2 minuten 4 keer per dag);
- acupunctuur (1-2 keer per week naar een richtpunt of gebied) waar geen infectie is *.
Er is een klein aantal onderzoeken gewijd aan het effect van magnetische velden op tumoren en aan het verbeteren van de primaire therapie. Een beperkt aantal publicaties heeft melding gemaakt van een afname van de tumorgroeisnelheid bij dieren onder invloed van een pulserend constant magnetisch veld. De theoretische basis voor een dergelijke therapie is echter nog niet ontwikkeld. De redenen voor dit effect zijn onduidelijk, de bijwerkingen zijn onbekend en er zijn veel theorieën over het behandelprotocol.
Geneesmiddelresistentie overwinnen. Therapeutische middelen zijn effectief wanneer ze worden gestart bij 90% van de gevallen van primaire borstkanker en bij 50% van de gevallen van gemetastaseerde borstkanker. Na een bepaalde periode keert de ziekte echter terug in 30% van de gevallen van primaire kanker. In dit geval is behandelingsresistentie niet alleen gebruikelijk, maar ook te verwachten. Als er eenmaal metastase optreedt, is de kans op genezing zeer beperkt. Het gemiddelde vijfjaarsoverlevingspercentage voor deze patiënten bedraagt 20%, en de gemiddelde levensverwachting varieert van 12 tot 24 maanden *. De mechanismen van de resistentie van kankercellen tegen elk medicijn kunnen verschillen *.
Aangenomen wordt dat de belangrijkste reden voor terugval de aanwezigheid van kankerstamcellen is, die worden gekenmerkt door resistentie tegen chemotherapie, bestraling en andere behandelingen *. Er zijn veel genetische en cellulaire aanpassingen die CSC’s resistent maken tegen veelgebruikte therapieën. Dit is in het bijzonder een toestand van relatieve rust en langzame celcyclus; verminderde absorptie van chemotherapiemedicijnen; hoge activiteit van membraantransporters en aldehydedehydrogenase; effectief DNA-herstel; expressie van anti-apoptotische eiwitten; weerstand tegen oxidatieve stress en enkele andere *.
Sommige stoffen maken het via verschillende mechanismen mogelijk om de geneesmiddelresistentie van cellen tegen te gaan, waardoor hun gevoeligheid voor chemotherapeutische middelen wordt verergerd.
• Metformine vermindert de energietoevoer van transportpompen (zoals P-glycoproteïne *) die giftige stoffen uit de cel pompen, waardoor de werking van andere therapeutische middelen wordt versterkt. De combinatie van doxorubicine en metformine doodt niet alleen grote hoeveelheden tumorcellen, maar ook borstkankerstamcellen *, en roeit tumoren bij muizen vrijwel uit.
De combinatie van metformine met aspirine in vitro (bij 10+5 mM) heeft een sterke synergetische onderdrukking van de tumorgroei door de onderdrukking van de anti-apoptotische eiwitten Mcl-1 en Bcl-2 en de activering van de pro-apoptotische eiwitten Bim en Puma. Intraperitoneale injecties van metformine (200 mg/kg) met aspirine (60 mg/kg) drie keer per week gedurende 28 dagen verminderden de groei van de pancreastumor bij muizen met drie keer vergeleken met de controle *. In menselijke equivalenten zou dit 1'500 mg metformine en 400 mg aspirine zijn.
• Thymoquinone vermindert het vermogen om beschadigde DNA-moleculen te repareren en verzwakt de resistentie tegen geneesmiddelen. Bij muizen veroorzaakte thymoquinone (100 mg/kg) DNA-schade in leukemiecellen (WEHI-3) door stilstand van de celcyclus in de S-fase *. Patiënten met gemetastaseerde of voorbehandelde borstkanker die thymoquinone (1-10 mg/dag) gebruikten, verminderden de tumormarkers met 25% ten opzichte van de uitgangswaarden gedurende 2 weken *. Thymoquinone werd goed verdragen bij doses tot 2'600 mg/dag en vertoonde geen toxiciteit of bijwerkingen.
• Sulindac, een niet-steroïde anti-inflammatoir geneesmiddel (600 mg), kan de multimedicijnresistentie-membraanpomp MRP1 remmen, waardoor de effecten van epirubicine bij patiënten tegen verschillende soorten kanker worden versterkt *.
• Aminazine (chloorpromazine) en acepromazine remmen in lage concentraties in vitro (bij 0,9 μM) de activiteit van het heat shock-eiwit HSP27 * * *. Met colontumor geënte muizen die werden behandeld met chloorpromazine-injecties (10 mg/kg elke 2 dagen gedurende 2 weken) vertraagden de snelheid van de tumorgroei met de helft *.
• Noscapine is een opioïde antitussivum dat de resistentie tegen doxorubicine bij muizen helpt overwinnen (300 mg/kg) en de groei van TNBC-tumoren 3-4 maal remt *. Noscapine en zijn analogen blokkeren de celdeling door tubuline te binden tijdens mitose. Uit onderzoek bij knaagdieren bleek dat noscapine en twee andere noscapine-analogen alleen de groei en overleving van geënte tumoren significant remden zonder enige detecteerbare toxiciteit * *. Het is zeer waardevol dat noscapine, in tegenstelling tot standaard chemotherapeutica, het immuunsurveillancesysteem niet verstoort, zoals kan worden beoordeeld aan de hand van het onveranderde aantal B- en T-cellen onder de onbehandelde en met noscapine behandelde groepen.
• Wogonin vermindert de activiteit van het heat shock-eiwit HSP90 en de niveaus van zijn cliënteiwitten (zoals EGFR, CDK4 en Survivin *). Experimenten met muizen toonden de activiteit van wogonine aan bij het onderdrukken van de angiogenese van getransplanteerde borsttumoren (equiv. 10 mg/kg) *.
• Simvastatine en andere statines in vitro (bij 20 μM) activeren de pro-apoptotische genen Bax en onderdrukken de anti-apoptotische genen Bcl-2 en Survivin in abnormale en kankerachtige borstcellen *.
• Silibinine (bij 200-400 μM), CAPE (bij 25 μM) en vitamine C (bij 1 mM) verminderen de productie van intracellulaire energie in vitro door de aerobe ademhaling te blokkeren, wat de vorming van de mammosfeer van ER+-tumoren aanzienlijk onderdrukt *.
• Salinomycine is een ionofoor antibioticum dat de membraanpomp ABCB1 (P-glycoproteïne) sterk remt *. Het vermindert ook de in vitro (bij 1 μM) c-FLIP-expressie en induceert apoptose door activering van de doodsreceptor DR5*.
• Piperine, capsaïcine *,resveratrol *, EGCG * * en andere polyfenolen * * * * onderdrukken in vitro ook de transportactiviteit van P-glycoproteïne, maar onvergelijkbaar zwakker. Piperine is ook een sterke MRP1-remmer *.
• Myricetine remt ook in vitro (bij 20 μM) * de multimedicijnresistentie-eiwitten MRP1/MRP2.
• Curcumine *,berberine *, EGCG *, evenals flavonoïden die fungeren als natuurlijke AHR-liganden (kaempferol, chrysine, genisteïne, naringenine) kunnen worden gebruikt om de BCRP-membraanpomp (Breast Cancer Resistance Protein) te remmen * * *.
• Tinospora (Tinospora cordifolia). Tinospora-dichloormethaanextract remt de ABC-transporters aanzienlijk en is zeer effectief tegen geneesmiddelresistente cellen van verschillende epitheliale tumoren *.
• Disulfiram en andere ALDH-remmers maken in vitro cellen gevoelig voor chemotherapiemedicijnen, met name cyclofosfamide * en gemcitabine *.
• Celecoxib voorkomt in vitro de activering van de Akt/Survivin-route, die apoptose en autofagie remt *.
• Epigallocatechinegallaat (EGCG) is in vitro (bij 50 μM) een natuurlijke remmer van HSP90 *.
Borst-CSC's zijn, ongeacht hun klinische subtypes en heterogeniteit van de tumor, uiterst gevoelig in vitro voor het verzwakken van de repressie van de proapoptotische TRAIL-route *.
• Magnolol onderdrukt de NF-signaalroute en activeert proapoptotische signalen, waaronder DR5, Bax en caspase-3 *. De combinatie van magnolol met een ander magnoliapolyfenol, honokiol (20+20 mg/kg), werkt synergetisch en vermindert meerdere malen de ontwikkeling van geënt glioom bij muizen *.
• Butyraat verhoogt de expressie van de doodsreceptor DR5 *. Als exogeen additief vertoont natriumbutyraat een slechte stabiliteit; het niveau van endogeen butyraat kan echter worden verhoogd door de darmmicroflora te normaliseren door butyraatproducerende bacteriën te voeden met plantaardige vezels.
Het overwinnen van intratumorale druk. Ontsteking geassocieerd met de tumor veroorzaakt verhoogde capillaire lekkage, en de verhoogde hoeveelheid lymfevocht verhoogt de lokale hydrostatische druk in de tumor. Bovendien vormt tumorangiogenese defecte bloedvaten, die ook worden gekenmerkt door lekken, en nog meer defecte lymfevaten die hun functies niet goed aankunnen. Verhoogde permeabiliteit van de vaatwand, samen met een afname van de lymfatische functie, leidt tot een toename van de intercellulaire druk in de tumor.De verhoogde druk in de tumor, evenals de verhoogde stijfheid ervan, creëert een micro-omgeving die de celproliferatie * bevordert en de invasiviteit * van tumorcellen vergroot.
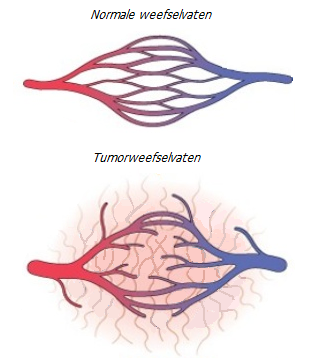
Bovendien verhinderen fibrose, slechte vloeistofcirculatie en verhoogde intratumorale druk dat therapeutische middelen op natuurlijke wijze diep in de tumor doordringen en hebben ze ook de neiging deze naar buiten te duwen. Dit is een van de belangrijkste redenen waarom tumorbehandelingen met verschillende chemicaliën mislukken. We kunnen de meest effectieve medicijnen in vitro maken, maar het probleem om ze op het beoogde doel af te leveren kan hen volledig beroven van hun vermogen om de tumor te bestrijden.
Om dit probleem te overwinnen kunnen therapeutische medicijnen rechtstreeks in de tumor worden geïnjecteerd. Lokale gerichte toediening kan de bijwerkingen van de therapie aanzienlijk verminderen en de effectiviteit ervan vergroten. Invasieve methoden kunnen injecties en/of katheters omvatten, evenals intratumorale capsules die langzaam therapeutische middelen afgeven. Helaas verstoren traumatische methoden van medicijntoediening de integriteit van het basaalmembraan, en dit helpt alleen maar de verspreiding van tumorcellen.
Meer de voorkeur verdienen niet-invasieve methoden voor intratumorale toediening van therapeutische middelen, die gebaseerd zijn op het overwinnen van hydrostatische druk met behulp van druk van een andere aard. Dit zou bijvoorbeeld sonoforese kunnen zijn, dat wil zeggen het vergroten van de permeabiliteit van weefsel onder invloed van akoestische energie van ultrageluid. Dit kan ook iontoforese * zijn, dat wil zeggen de afgifte van een medicijn aan de tumor, niet langs een concentratie- of drukgradiënt, maar onder invloed van gelijkstroomenergie. Iontoforese is een oude, bewezen technologie die met succes wordt toegepast op andere gebieden van de geneeskunde, maar de laatste jaren ook wordt gebruikt in experimenten tegen kwaadaardige tumoren * *.
Lokale toediening van actieve middelen maakt het mogelijk dat ze bij het doel worden afgeleverd zonder eerst door de lever te gaan, en om hun concentratie te verhogen zonder de belasting van andere organen en weefsels te vergroten, waardoor de negatieve bijwerkingen worden verminderd. Beide veelbelovende methoden zijn echter nog niet in de wijdverbreide oncologische praktijk geïntroduceerd. Eén obstakel hiervoor is het feit dat transcutane elektroforese therapeutische concentraties kan opleveren binnen enkele millimeters van de elektrode. Dit zou gunstig kunnen zijn bij huidmaligniteiten, maar het bereik van de therapeutische middelen in de borstcellen met behulp van klassieke elektroforese is twijfelachtig.
De oplossing voor dit probleem ligt in het injecteren van werkzame stoffen, niet in de tumor zelf, maar in de onmiddellijke omgeving ervan, en deze vervolgens onder invloed van elektroforese te dwingen in de tumor binnen te dringen. Maar dit blijft nog steeds een kwestie van gedurfde voorstellen.
Elektroforese kan effectiever zijn als de werkzame stoffen niet rechtstreeks door de huid en het weefsel worden gedwongen, maar langs directe vaatstelsel, in het bijzonder langs de melkkanalen. Deze aanpak kan nuttig zijn bij de ziekte van Paget. Voor diepe toediening in de borstklier moeten therapeutische middelen eerst via de tepel in de kanalen worden geïnjecteerd.
Transductale elektroforese zou vermoedelijk nuttig kunnen zijn in de volgende gevallen:
• Preoperatieve behandeling van de borstklier – door het weefsel te verzadigen met nauwkeurig afgemeten doses progesteron, doxycilline of andere stoffen die de uitkomst van een daaropvolgende operatie kunnen verbeteren.
• Postoperatieve behandeling – door de introductie van ontstekingsremmende en herstellende stoffen, antioxidanten en vitamines, evenals claritromycine, diclofenac, jodium, vitamine D, retinoïnezuur.
• Tijdens algemene chemotherapie, in niet-gevorderde gevallen van primaire borsttumoren, zou lokale toediening van vasodilatatoren en stromale modificatoren, waaronder proteolytische enzymen, de verzadiging van het doelweefsel met het primaire therapeutische middel kunnen verbeteren.
Om kankerstamcellen te vernietigen – salinomycine of niclosamide, metformine, itracosanol, disulfiram, diclofenac, vitamine D, retinoïnezuur.
• Tijdens bestralingstherapie zou lokale verzadiging van weefsel met zuurstof, ijzer- en koperionen en andere oxidatiemiddelen mogelijk de door straling geïnduceerde oxidatieve stress kunnen verhogen, waardoor de therapeutische kracht van ioniserende straling kan worden verzwakt.
Als aanvulling op bestralingstherapie – paracetamol, metformine, diclofenac, dibazol.
Voor weefselherstel na bestralingstherapie – resveratrol, curcumine.
• Tijdens de periode tussen de therapieën kan elektroforese de extracellulaire zuurgraad van een glycolytische tumor reguleren, waarbij ionen van alkalische elementen, waaronder rubidium en cesium, in de tumor en in de directe omgeving worden afgegeven.
Om de resterende kankercellen van de tumormassa te vernietigen – viscumine, baicaleïne, tanshinon, parthenolide.
Als glycolyseremmers – wogonine, clotrimazol.
Als remmers van OF – doxycycline, azitromycine, metformine.
Als ontstekingsremmende middelen – curcumine, acetylsalicylzuur en boswellinezuur.
• In alle gevallen kunnen dimethylsulfoxide, dexamethason en dibazool als versterkers worden gebruikt.
Ondanks de belofte ervan bevindt een dergelijke therapie zich nog steeds in het stadium van theoretische ontwikkeling.
Nanodragers. Een ideaal medicijnafgiftesysteem moet de stabiliteit van het medicijn garanderen, gericht op een bepaalde plaats in het lichaam en gecontroleerde afgifte na aflevering op de eindbestemming.
Eenmaal in het lichaam geïntroduceerd, moeten therapeutische middelen een aantal obstakels overwinnen voordat ze hun doel kunnen bereiken. Ze moeten intact blijven, binding en verwijdering uit het lichaam vermijden, opname door immuuncellen vermijden, zich in voldoende hoeveelheden ophopen in hun doelwit, en pas daarna kunnen ze hun therapeutische effect manifesteren.
En wanneer ze oraal worden ingenomen, moeten ze eerst de darmwand in de bloedbaan doordringen, wat bepaalde problemen oplevert voor hydrofobe stoffen. Het is niet verrassend dat veel stoffen die in vitro effectief zijn, in klinische onderzoeken totaal niet indrukwekkend blijken te zijn.
De afgelopen jaren is de onderzoeksinteresse verschoven naar de creatie van nanodragers als een veelbelovend mechanisme voor medicijntransport. De effectiviteit van nanocarriers als medicijnafgiftesystemen hangt sterk samen met hun structuur en kenmerken.
Vereisten voor nanodeeltjes.
De grootte van nanodragers is belangrijk voor hun beweging door de bloedbaan en de levering aan tumorweefsel *. Het optimale bereik van nanodeeltjesgroottes is 30-200 nm. Nanodeeltjes met een diameter van 100-150 nm hebben een 4-6 maal hogere tumoropname dan deeltjes met een diameter kleiner dan 30 nm of groter dan 300 nm *.
Er is waargenomen dat deeltjes kleiner dan 20-30 nm snel via de nieren kunnen worden uitgescheiden; deeltjes groter dan 50 nm passeren de bloed-hersenbarrière niet goed; deeltjes groter dan 100 nm hebben de neiging zich op te hopen nabij de wanden van het vat; deeltjes groter dan 200 nm dringen zwak het tumorendotheel binnen; deeltjes groter dan 3 micron zijn onderhevig aan verbeterde fagocytose; en deeltjes groter dan 4 micron kunnen worden vastgehouden in de kleinste haarvaten van het vaatstelsel * *. In het bereik van 120-200 nm worden nanodeeltjes niet waargenomen door de cellen van het reticuloïde endotheliale systeem en vermijden daarom snelle filtratie door de lever en de milt *.
Het zetapotentiaal wordt bepaald door de lading op het oppervlak van deeltjes die zijn gesuspendeerd in een colloïdale oplossing, namelijk bloed. Hoe negatiever de waarde van deze indicator, hoe sterker de deeltjes elkaar afstoten, hoe minder hun neiging tot agglomeratie en hoe hoger hun stabiliteit. Aan de andere kant worden deeltjes met een kleine positieve lading sneller door cellen opgenomen. De ζ-potentiële waarde van de nanodrager van -30 mV tot +5 mV wordt als acceptabel beschouwd.
Biocompatibiliteit en biologische afbreekbaarheid van materialen zijn ook belangrijk voor de effectiviteit van therapie.
Klassen van nanodragers. De meest voorkomende materialen zijn eiwitten, cyclodextrinen, liposomen, polymeren, polymeer-lipide-hybriden, dendrimeren, hydrogels, faseveranderingsmaterialen en anorganische materialen. Elk van hen heeft zijn voor- en nadelen. Laten we eens kijken naar de meest eenvoudig te implementeren ervan.
Cyclodextrinen zijn koolhydraten van ongeveer 70 nm met een conische moleculaire structuur met een lipofiel interieur en een hydrofiele buitenkant. Dankzij dit ontwerp kunnen hydrofobe stoffen verborgen worden in het binnenste deel van cyclodextrinen, waardoor hun biologische beschikbaarheid wordt verbeterd. Het laden van cyclodextrinen is uiterst eenvoudig en hun capaciteit neemt af in de volgende volgorde: 2-hydroxypropyl-β-cyclodextrine ⇒ methyl-β-cyclodextrine ⇒ β-cyclodextrine ⇒ γ-cyclodextrine *. Ondanks al hun voordelen zijn cyclodextrinen geen gesloten containers en kunnen ze net zo snel hun inhoud verliezen.
Liposomen zijn bollen gevormd door een lipidedubbellaag die lijkt op een celmembraan. Liposomale structuren zijn gemakkelijk te produceren en maken het transport mogelijk van zowel hydrofiele stoffen (in het binnencompartiment) als lipidofiele stoffen (in de laag). De liposoomtechnologie produceert echter relatief grote deeltjes (groter dan 200 nm).
Vaste lipide-nanodragers zijn bollen met een enkellaagse lipidelaag die therapeutische middelen omringt. Deze technologie produceert, vergeleken met liposomen, doorgaans kleinere deeltjes (50-200 nm) met een hogere concentratie aan getransporteerde stoffen. Het is niet alleen geschikt voor injectie, maar ook voor orale toediening, maar kan alleen lipidofiele moleculen laden.
Hoewel de lipiden zelf biocompatibel en niet-toxisch zijn, vereist de technologie voor het bereiden van lipideschillen vaak organische oplosmiddelen. Als alternatief kan homogenisatie worden gebruikt, maar dit vereist processen met hoge energie, zoals extrusie onder hoge druk, langdurig (tot 3 uur) mengen met hoge afschuiving of langdurige ultrasone trillingen van het vloeibare mengsel.
Omdat nanodeeltjes een hoge permeabiliteit vertonen, inclusief penetratie door de bloed-hersenbarrière, worden speciale eisen gesteld aan de zuiverheid van de gebruikte grondstoffen en technologieën.
Modificaties van nanodragers. Het vrijkomen van de inhoud van lipide-nanodeeltjes vindt plaats door erosie van de lipide-omhulling en diffusie van hun inhoud. Zonder aanvullende verbeteringen vertonen lipidestructuren instabiliteit en worden ze bovendien snel gedetecteerd door macrofagen. Het coaten van liposomen met polyethyleenglycol (5-10%) of soortgelijke stoffen verhoogt hun stabiliteit en maskeert aanvankelijk de liposomen voor herkenning door immuuncellen.
De targeting van nanodragers kan worden verbeterd door liganden aan hun oppervlak te hechten die zeer specifiek zijn voor receptoren en andere doelwitten die specifiek tot overexpressie komen op het oppervlak van borstkankercellen. Dit kunnen bijvoorbeeld oestriol, hyaluronzuur, folaten en retinoïden zijn.
De folaatreceptor komt in overexpressie op TNBC-cellen, dus folaatbevattende liposomen zullen beter worden opgenomen door kankercellen *. En hyaluronzuur functioneert tegelijkertijd als een hydrofiele stabilisator en als een molecuul dat een hoge affiniteit vertoont voor de CD44-receptor (transmembraanglycoproteïne type 1), waarvan de expressie verhoogd is in kankercellen * *.
Het gebruik van materialen in de nanocarrier-omhulling die onstabiel zijn onder hypoxie en/of hyperaciditeit (zoals waargenomen in tumorweefsel) kan de effectiviteit van therapieën die hun doel bereiken verder verbeteren. Tumorcellen zijn echter niet de enige cellen in het lichaam die zich delen onder zeer zure omstandigheden. Daarom zou het voordeliger zijn om materialen te gebruiken die reageren op gecontroleerde externe invloeden, zoals licht, ultrageluid, temperatuur, elektromagnetisch veld, enz.
Verhoogde permeabiliteit van tumorvatwanden, gekoppeld aan slechte lymfedrainage, kan passieve tumorinfiltratie en daaropvolgende retentie van in nanodeeltjes ingekapselde therapieën bevorderen. Het is echter onwaarschijnlijk dat de toediening van middelen aan opkomende kleine tumoren die geen afwijkingen in de groeiende bloedvaten vertonen, voordeel zal halen uit het effect van vasculaire lekkage.
Nanodragers worden al in klinische omgevingen gebruikt, waardoor de effectiviteit van veel chemotherapiemedicijnen * wordt vergroot en de bijwerkingen ervan worden verminderd. Vanwege hun succes wordt een verdere groei in het gebruik van nanodragers verwacht.
Een voorbeeld van de bereiding van nanodeeltjes geladen met curcumine op basis van cyclodextrine.
Bèta-cyclodextrine (40 mg) wordt opgelost in 8 ml gedeïoniseerd water in een glazen houder van 20 ml, waarbij 40 ml van een 30% oplossing van curcumine in een organisch oplosmiddel (bij voorkeur ethylalcohol) wordt toegevoegd. Het resulterende mengsel werd een nacht zonder deksel bij 400 rpm geroerd om het oplosmiddel te verdampen. Bewaren in het donker bij 4°C gedurende meerdere dagen *.
Dergelijke nanodeeltjes kunnen de oplosbaarheid van curcumine 180 keer verhogen *, maar ze beschermen curcumine niet tegen snelle metabolisatie.
Een voorbeeld van de bereiding van met curcumine beladen lipide nanodeeltjes met behulp van hete homogenisatie met hoge afschuiving.
Curcumine wordt kant-en-klaar ingenomen of geëxtraheerd uit kurkumapoeder met behulp van een Soxhlet-extractor, waarbij dichloormethaan als oplosmiddel wordt gebruikt (of andere oplosmiddelen vermeld in volgorde van afnemende oplosbaarheid: aceton ⇒ ethylacetaat ⇒ methanol ⇒ chloroform ⇒ ethanol ⇒ dichloorethaan ⇒ isopropanol ⇒ ether ⇒ benzeen ⇒ hexaan). Van deze hele lijst lijkt ethanol het meest acceptabel. De opbrengst aan het droge eindproduct na verwijdering van het oplosmiddel moet 2-5% van het gewicht van de oorspronkelijke grondstof bedragen.
Nanoliposomen worden geproduceerd zonder het gebruik van oplosmiddelen, door twee vooraf bereide delen te homogeniseren: lipiden en water in een gewichtsverhouding van 0,1-30%. In dit geval bevat het waterige deel 0,5-5% stabiliserende oppervlakteactieve stoffen.
Om het lipidegedeelte te bereiden, kunt u glycerylmonooleaat (500 mg) als vast lipide en olijfolie (25 mg) als vloeibaar lipide nemen. De lipiden worden in een glazen vat in een waterbad tot 80 °C verwarmd, waarna, grondig gemengd, 5 mg curcumine wordt toegevoegd, evenals 80 mg lecithine als hulpemulgator.
Om het waterige deel te bereiden, wordt 200 mg polysorbaat 80 (Tween 80) per 50 ml dubbel gedestilleerd water als belangrijkste emulgator genomen en dit mengsel wordt verwarmd tot 75 °C. Het hete waterige deel wordt beetje bij beetje aan het lipidedeel toegevoegd, waarbij het wordt afgebroken met behulp van een homogenisator bij 12'000 rpm gedurende 15 minuten bij een temperatuur van 75-80 °C. De resulterende dispersie wordt snel afgekoeld in een ijsbad en overgebracht naar een vriezer (-20 °C) om volledig af te koelen. Bewaren bij +4 °C op een donkere plaats gedurende maximaal een maand. Dosering: 30 g/dag, d.w.z. ongeveer 2 eetlepels/dag.
De gemiddelde grootte van de resulterende nanodeeltjes moet 110 nm zijn bij een ζ-potentiaal van -44 mV; inkapselingsefficiëntie – 75%; en het laadvolume van curcumine in het liposoom is ongeveer 1%. De IC50-waarde tegen ER-positieve kankercellen (MCF-7) voor nanodeeltjes kan meer dan 20 keer toenemen in vergelijking met pure curcumine *. Bestraling van cellen met blauw licht (420-430 nm) vergroot deze kloof nog verder.
Als alternatief kunt u voor het lipidegedeelte visolie, eucalyptus- of sandelhoutolie gebruiken in plaats van olijfolie. Het lipidegedeelte kan worden aangevuld met in vet oplosbare therapeutische middelen zoals retinol. Het waterige deel kan worden aangevuld met andere wateroplosbare stoffen zoals hyaluronzuur of foliumzuur (200 μg).
Als de snelheid van de homogenisator wordt verlaagd tot 5'000 rpm, moet de procedure worden verlengd tot 1,5 uur. In plaats van homogeniseren kan een ultrasone behandeling gedurende 1-2 uur worden toegepast met continu roeren, frequentie 40 kHz en intensiteit 15 W/cm2. Eventuele afwijkingen van de hierboven beschreven technologie kunnen de kenmerken en effectiviteit van nanodeeltjes echter aanzienlijk veranderen.
Een voorbeeld van de bereiding van lipide-nanodeeltjes geladen met curcumine met behulp van hete homogenisatie en ultrasoon * * *.
Om het lipidegedeelte te bereiden, mengt u 120 mg cetylpalmitaat (plantaardige spermaceti) en 180 mg oliezuur en verwarmt u deze tot een temperatuur 5 °C boven het smeltpunt van cetylpalmitaat. Vervolgens wordt 15 mg pure curcumine onder voortdurend roeren opgelost in de hotmelt. Om het waterige gedeelte te bereiden, lost u 200 mg polysorbaat (Tween 80) op in 10 ml dubbel gedestilleerd water en verwarmt u tot de temperatuur van het lipidegedeelte (optioneel plus 100 μg foliumzuur).
Vervolgens wordt de hete waterige oplossing, onder voortdurend roeren en met handhaving van de begintemperatuur, druppelsgewijs aan het lipidegedeelte toegevoegd en gedurende 3 minuten bij een rotatiesnelheid van 11'000 rpm gehomogeniseerd, waarbij grote lipidedeeltjes (ongeveer 3 μM) worden verkregen. Om de deeltjes verder te vermalen, wordt het mengsel gedurende 20 minuten behandeld met ultrageluid met een specifiek vermogen van 100 W/l. Verkleining van de deeltjesgrootte vindt plaats onder invloed van turbulentie en cavitatie. Hierna wordt de oplossing onder voortdurend roeren overgebracht naar een ijsbad en snel afgekoeld tot kamertemperatuur.
De gemiddelde grootte van de resulterende nanodeeltjes zou 120-200 nm moeten zijn met een ζ-potentieel van ongeveer -30 mV. De inkapselingsefficiëntie bedraagt meer dan 80% bij een curcuminelading van 5%.
Een voorbeeld van de bereiding van met curcumine beladen lipide nanodeeltjes met behulp van met water mengbare organische oplosmiddelen.
Om het lipidegedeelte te bereiden, worden 150 mg curcumine, 200 mg stearinezuur en 100 mg lecithine met behulp van ultrageluid opgelost in 10 ml chloroform of ethanol. Om het waterige deel te bereiden, wordt 200 mg polyethyleenglycolmonostearaat opgelost in 30 ml dubbel gedestilleerd water. Beide delen worden verwarmd tot 75 °C.
Vervolgens wordt het gesmolten lipidegedeelte via een G23-injectienaald (diameter 0,6 mm) aan het hete watergedeelte toegevoegd, waarbij dit wordt geroerd met een snelheid van 1'000 rpm. In dit geval migreert het organische oplosmiddel naar het waterige deel, waardoor nanodeeltjes neerslaan. Het roeren wordt gedurende ongeveer 1 uur bij 75°C voortgezet. Tijdens deze behandeling verdampt het organische oplosmiddel volledig en wordt het volume van het mengsel dikker tot ongeveer 5 ml.
Hierna wordt de resulterende samenstelling onmiddellijk in een ijsbad (0-2 °C) geplaatst en wordt 5 ml koud water toegevoegd, waarbij gedurende 2 uur wordt geroerd met een snelheid van 1'200 rpm * *.
De gemiddelde deeltjesgrootte moet 40 nm zijn bij een ζ-potentiaal van -50 mV. De efficiëntie van het laden en inkapselen van geneesmiddelen is respectievelijk 23% en 72%. IC50 is 1,5 keer hoger dan pure curcumine. Dosering: 5 g/dag, d.w.z. ongeveer 1 theelepel/dag.
Over het algemeen zou de voltooide compositie ongeveer moeten bevatten:
• 80% dubbel gedestilleerd water;
• 10% vaste lipiden (cetylpalmitaat, bijenwas);
• 4% vloeibare lipiden (oliezuur, olijfolie, reuzel, kokosolie, lijnzaadolie, sandelhoutolie, visolie);
• 5% emulgatoren (polysorbaat-80, sojalecithine, eilecithine);
• 1% actief ingrediënt (curcumine, quercetine, resveratrol, retinol, enz.).
De kenmerken van nanodeeltjes zullen echter sterk variëren, afhankelijk van de gebruikte componenten, en voldoen mogelijk niet aan de vereiste voorwaarden.
Ter afsluiting van de bespreking van de middelen en methoden voor het vernietigen van kankercellen merken we op dat, hoe voortreffelijk de successen op dit gebied ook mogen zijn, het alleen maar wegwerken van kankercellen niet betekent dat de ziekte wordt kwijtgeraakt. Kankercellen zijn slechts een manifestatie van het probleem, maar niet de essentie ervan *.